La Agencia Europea del Medicamento aprueba el remdesivir como primer fármaco para tratar el COVID-19
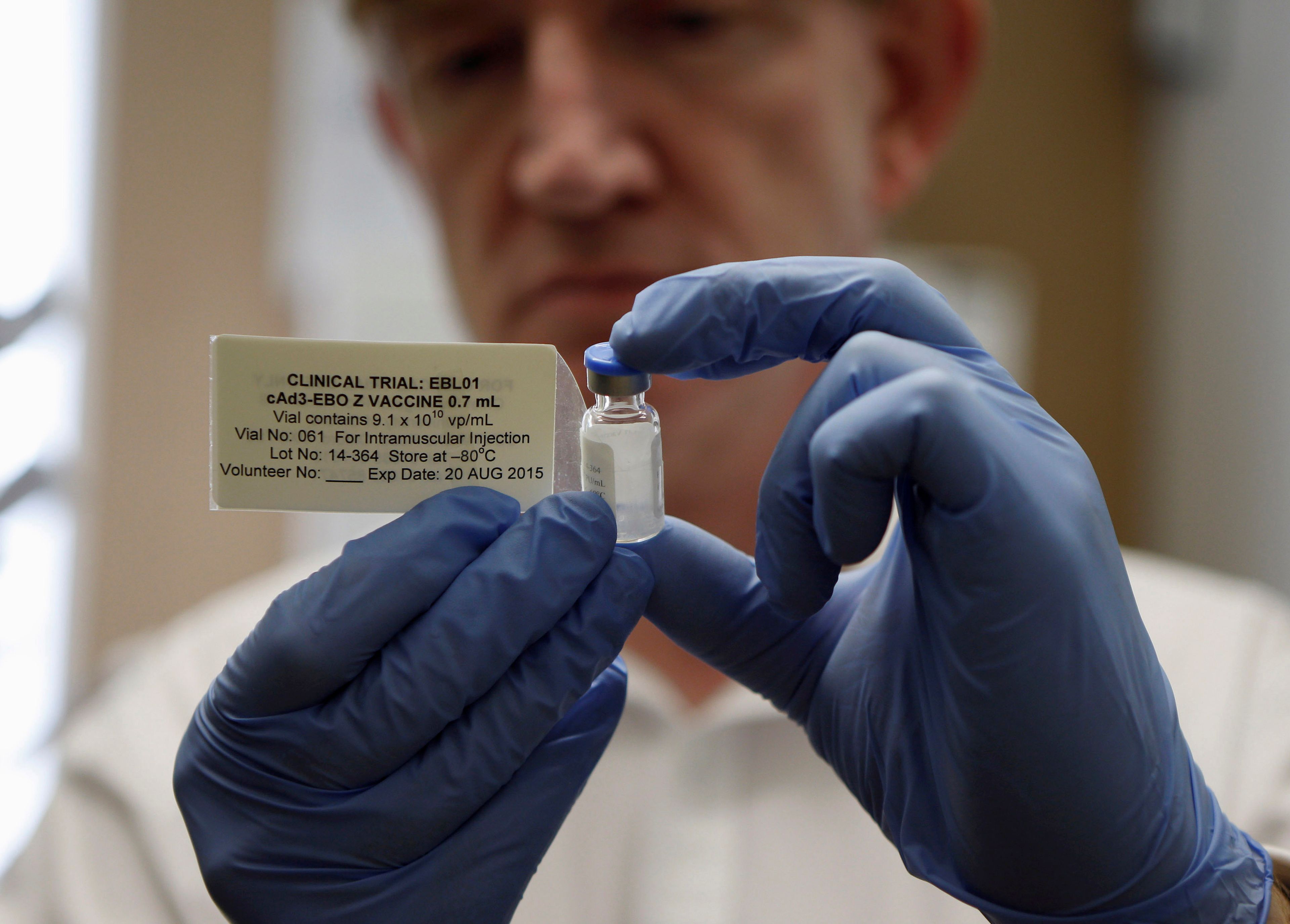
- La Agencia Europea del Medicamento (EME) ha autorizado el uso del remdesivir para tratar a pacientes con COVID-19 después de que su comité científico le haya dado el visto bueno.
- Se empezará a comercializar en cuanto la Comisión Europea apruebe el parecer de la EME y se aplicará en los hospitales por vía intravenosa.
- El ensayo ha demostrado que los pacientes graves tratados con remdesivir se recuperan de media en 12 días, seis días antes de que el resto.
- Descubre más historias en Business Insider España
La Agencia Europea del Medicamento (EME) ha autorizado el uso del remdesivir, el tratamiento antiviral de Gilead Sciences, para tratar a pacientes con COVID-19.En un comunicado, el organismo ha anunciado que recomienda autorizar su comercialización condicional después de recibir el visto bueno de su comité científico.
Gracias a la aprobación de la EME los médicos podrán recetar por primera vez un medicamento que alivie los malestares provocados por el coronavirus. En Europa adoptará el nombre de Veklury y su comercialización comenzará en cuanto la Comisión Europea de visto bueno a la recomendación de la EME, cuyo criterio suelen seguir políticos europeos.
La luz verde se ha conseguido después de que el medicamento pasara una estricta evaluación por parte de la EME que se llevó a cabo "en un periodo excepcionalmente corto". "A partir del 30 de abril de 2020, el Comité de Medicamentos de Uso Humano comenzó a evaluar los datos sobre la calidad y la fabricación, datos no clínicos, datos clínicos preliminares y datos de seguridad de apoyo de programas de uso compasivo. Mucho antes de la presentación de la solicitud de autorización de comercialización del 5 de junio", afirma la EME en su comunicado .
El Remdesivir ya había sido aprobado para uso de urgencia en pacientes con enfermedades graves en los Estados Unidos, India y Corea del Sur, y ha recibido la aprobación total en Japón.
Según la Agencia, el ensayo ha demostrado que los pacientes graves tratados con remdesivir se recuperan de media en 12 días, seis días antes de que el resto. Por el contrario, no se detectó ningún beneficio entre los pacientes menos graves ni en los pacientes que ya estaban con ventilación cuando empezaron a recibir el remdesivir.
Leer más: Este medicamento experimental está ayudando a que los pacientes se recuperen
La Agencia europea todavía tiene pendiente analizar los datos sobre mortalidad en pacientes tratados con remdevisir. "Teniendo en cuenta los datos disponibles, la Agencia considera que el equilibrio entre los beneficios y los riesgos ha demostrado ser positivo en pacientes con neumonía que necesitan oxígeno suplementario”, afirma en el comunicado.
El medicamento se suministrará por vía intravenosa en los hospitales bajo la supervisión del personal sanitario.
Otros artículos interesantes:
Descubre más sobre Iván Fernández, autor/a de este artículo.
Conoce cómo trabajamos en Business Insider.