Trasplantan cerebros cultivados en laboratorio a ratas con lesiones de la vista, y consiguen que respondan a la luz

Getty Images
- Científicos trasplantaron neuronas cultivadas en laboratorio al cerebro de ratas con la corteza visual dañada.
- Los resultados fueron asombrosos: al cabo de dos meses, las neuronas respondieron cuando las ratas veían luces intermitentes.
Un nuevo e increíble experimento nunca antes realizado se salda con resultados fascinantes: científicos de la Universidad de Pensilvania lograron trasplantar organoides cerebrales humanos a ratas para reparar lesiones en sus sistemas de procesamiento visual.
El nuevo estudio apunta al potencial de los minicerebros. Según los resultados, publicados en la revista Cell Stem Cell, resulta posible emplear modelos en miniatura cultivados en laboratorio de la superficie arrugada del cerebro humano para parchear lesiones en cerebros de ratas vivas. Gracias a ellos se pueden reparar conexiones rotas en los sistemas de procesamiento sensorial.
En un futuro no tan lejano, la idea de sus autores es que estos minicerebros —conocidos como organoides cerebrales— puedan utilizarse también para reparar cerebros de pacientes humanos.
Un nuevo avance acerca a humanos el trasplante de retinas artificiales para recuperar la visión
Los investigadores habían extirpado partes de la corteza visual de las ratas, con lo que su capacidad de visión había quedado muy mermada, pero gracias a estos minicerebros insertados en estas secciones deterioradas —algo parecido a un tapón cerebral-—, la corteza visual dañada pudo volver a la vida.
"Considero que este es el primer paso en el desarrollo de una nueva estrategia para reparar el cerebro", afirma el doctor Han-Chiao Isaac Chen, autor principal del estudio y profesor adjunto de neurocirugía en la Facultad de Medicina Perelman de la Universidad de Pensilvania.
En la siguiente imagen puede apreciarse el organoide cerebral trasplantado a la rata.
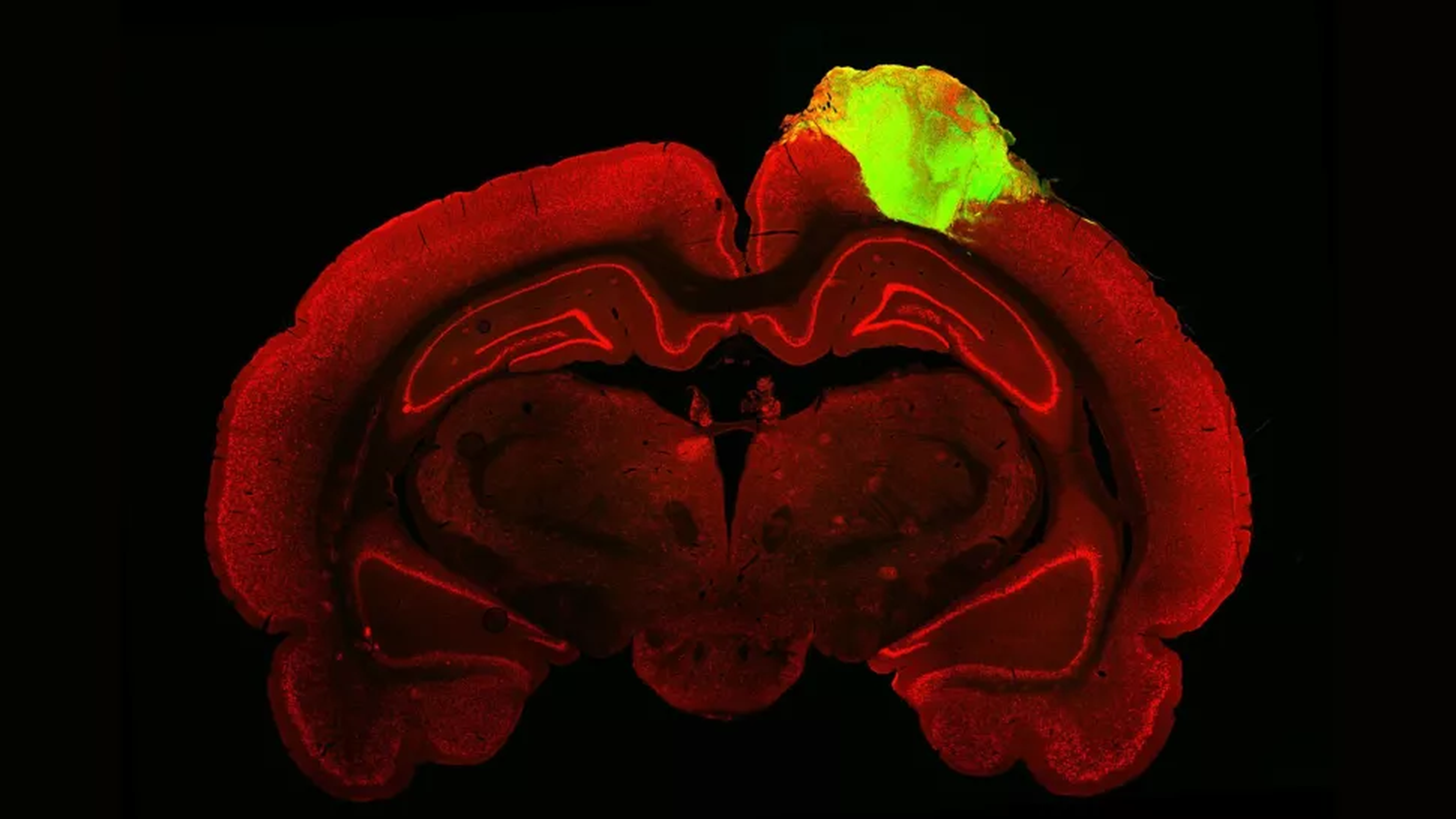
Jgamadze et al.
Lo que hace esta técnica es utilizar el organoide para tapar la lesión en el córtex visual secundario, donde se procesan los datos que la retina del ojo recibe con la luz, enviando un mensaje eléctrico a la corteza visual primaria.
Estudios previos permitieron trasplantar células cerebrales individuales en roedores sanos de distintas edades y organoides en cerebros de roedores muy jóvenes sin lesiones. Sin embargo, nunca hasta la fecha se había podido hacer con organoides en ratas mayores con lesiones.
Para cultivar estos minicerebros se partió de una célula madre humana, sometida a señales químicas durante 80 días para inducir a formar grupos tridimensionales que contenían muchos de los tipos celulares de la corteza cerebral humana, la capa externa arrugada del cerebro. El tejido tridimensional empezó a responder a estímulos al cabo de 1 meses e incluso creció un poco.
Los científicos mostraron a las ratas imágenes parpadeantes en una pantalla mientras medían la actividad neuronal mediante un electrodo implantado en sus cerebros. Con un líquido fosforescente especial en las zonas afectadas, pudo demostrarse que el organoide se conectó a las retinas de las ratas con una red de nuevas conexiones, respondiendo como un córtex visual normal.
Entre los potenciales efectos de esta tecnología aplicada dentro de unos años a seres humanos, recoge LiveScience, están la restauración de la función cerebral tras una lesión traumática, una cirugía invasiva o un ictus, o incluso para ayudar a combatir los efectos de enfermedades neurodegenerativas, como el párkinson.
Queda un largo camino por delante: los siguientes pasos serán cómo se ve afectada la visión de las ratas o qué nuevos materiales pueden imitar todavía mejor la forma del cerebro.
Otros artículos interesantes:
Descubre más sobre Andrea Núñez-Torrón Stock, autor/a de este artículo.
Conoce cómo trabajamos en Business Insider.