Dos nuevos tratamientos autorizados por la EMA para tratar el COVID-19: esto es todo lo que tienes que saber sobre Ronapreve y Regkirona
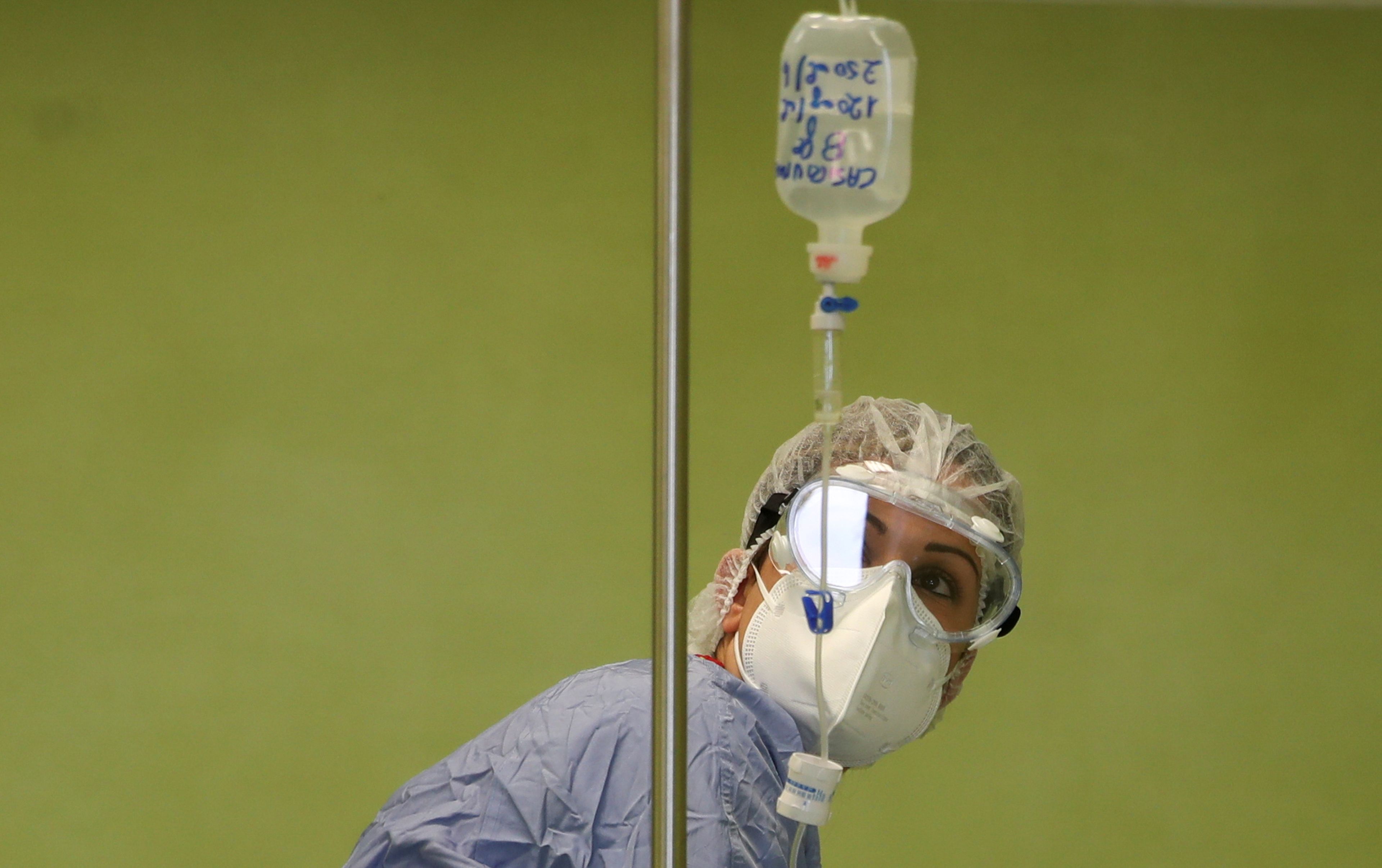
REUTERS/Yara Nardi
- La Agencia Europea del Medicamento (EMA) ha autorizado 2 nuevos tratamientos con anticuerpos monoclonales para el COVID-19: Regkirona y Ronapreve.
- Los tratamientos reducen significativamente las hospitalizaciones y muertes en pacientes con riesgo de enfermar gravemente tras la infección con el SARS-CoV-2.
- Descubre más historias en Business Insider España.
El comité de medicamentos humanos de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha autorizado los primeros anticuerpos monoclonales para el tratamiento del COVID-19, comercializados como Regkirona (regdanvimab) y Ronapreve (casirivimab/imdevimab).
Los anticuerpos monoclonales son sustancias químicas, versiones sintéticas de las proteínas del sistema inmunitario (anticuerpos), que se administran mediante inyecciones o transfusiones de sangre.
"Son proteínas diseñadas para unirse a un objetivo específico, en este caso la proteína de pico del SARS-CoV-2, que el virus usa para ingresar a las células humanas", explica la EMA.
El principal objetivo de este tipo de tratamientos es evitar que las personas con síntomas leves o moderados desarrollen un cuadro de enfermedad grave. Pero suelen requerir hospitalización y tienen un coste elevado para los sistemas públicos de salud, tal y como había informado Business Insidercon anterioridad.
En una anterior consulta de Business Insider España, farmacéuticos de los Servicios Técnicos del Consejo General de Farmacéuticos, Irene Suárez y Carlos Fernández Moriano, aclaran que estos probablemente no estén disponibles para todos los contagiados con el COVID-19.
"Habrá que ver en qué condiciones se autorizan y cómo se regula y prioriza su administración para conocer quiénes serán los subgrupos de pacientes que los recibirán primero".
"En cualquier caso, se debe subrayar que estos tratamientos no sustituirían a las vacunas, pero serían una herramienta más en la lucha frente al coronavirus para personas que ya se han infectado", añaden.
Hasta la fecha, el único fármaco con luz verde de la EMA para tratar la enfermedad que provoca el nuevo coronavirus SARS-CoV-2 era Veklury, más conocido como remdesivir.
"Se siguen investigando medicamentos para tratar el COVID, como los anticuerpos monoclonales. También se está trabajando en la investigación de antivirales para evitar la infección", revelaba en una entrevista con Business Insider España el presidente de la Sociedad Española de Inmunología, Marcos López Hoyos.
Ronapreve y Regkirona reducen significativamente las hospitalizaciones y las muertes en contagiados con riesgo de COVID-19 grave
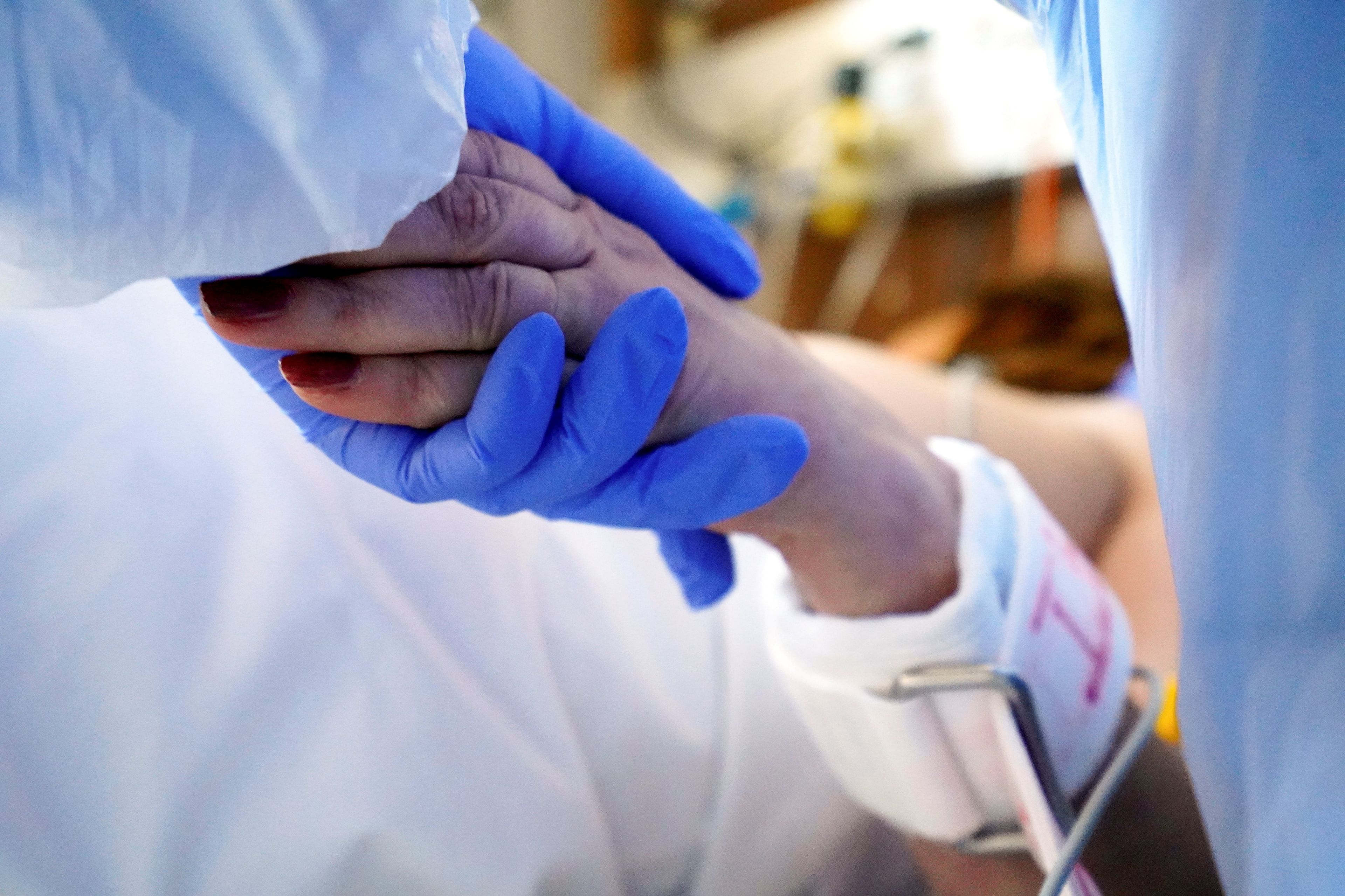
REUTERS/Janis Laizans
De acuerdo con el comunicado de la EMA, tanto Ronapreve como Regkirona reducen significativamente las hospitalizaciones y las muertes en pacientes con COVID-19 con riesgo de COVID-19 grave.
Pero Ronapreve también disminuye las posibilidades de contagio entre contactos cercanos.
En los ensayos de este último, el 0,9% de los pacientes tratados (11 de 1192 pacientes) fueron hospitalizados o murieron dentro de los 29 días de tratamiento en comparación con el 3,4% de los pacientes tratados con placebo (40 de 1193 pacientes).
Mientras que entre los contagiados con mayor riesgo de que su enfermedad se agrave, el 3,1% de los pacientes tratados con Regkirona (14 de 446) fueron hospitalizados, necesitaron oxígeno suplementario o murieron dentro de los 28 días de tratamiento en comparación con el 11,1% de los pacientes tratados con placebo (48 de 434).
El tratamiento desarrollado por Roche, Ronapreve, se ha autorizado para el tratamiento del COVID-19 en adultos y adolescentes —a partir de 12 años de edad y con un peso mínimo de 40 kilogramos— que no requieran oxígeno suplementario, pero que tengan un mayor riesgo de COVID-19 grave.
Se administra como una única perfusión (de goteo) en una vena dentro de los 7 días posteriores al inicio de los síntomas, en una dosis que varía según el peso del paciente.
Regkirona, de la mano de Celltrion Healthcare Hungary Kft, ha recibido luz verde para tratar a adultos infectados con el SARS-CoV-2 que no requieran oxígeno y que también tengan más riesgos de una evolución grave de la enfermedad que provoca el nuevo coronavirus.
También es de administración única en vena o mediante inyección debajo de la piel, dentro de los 7 días posteriores a la aparición de los síntomas. Pero tiene una dosis recomendada de 600 mg de casirivimab y 600 mg de imdevimab.
Conforme a las indicaciones de la Agencia, el perfil de seguridad de ambos medicamentos es favorable con un pequeño número de reacciones relacionadas con la perfusión —es decir, con la acción del líquido ingresando de manera lenta pero sostenida en el organismo—.
Otros artículos interesantes:
Descubre más sobre Kamila Barca, autor/a de este artículo.
Conoce cómo trabajamos en Business Insider.