Novavax dice que su vacuna contra el coronavirus ha resultado muy efectiva en su ensayo de Reino Unido, pero no ha funcionado igual de bien contra la variante sudafricana
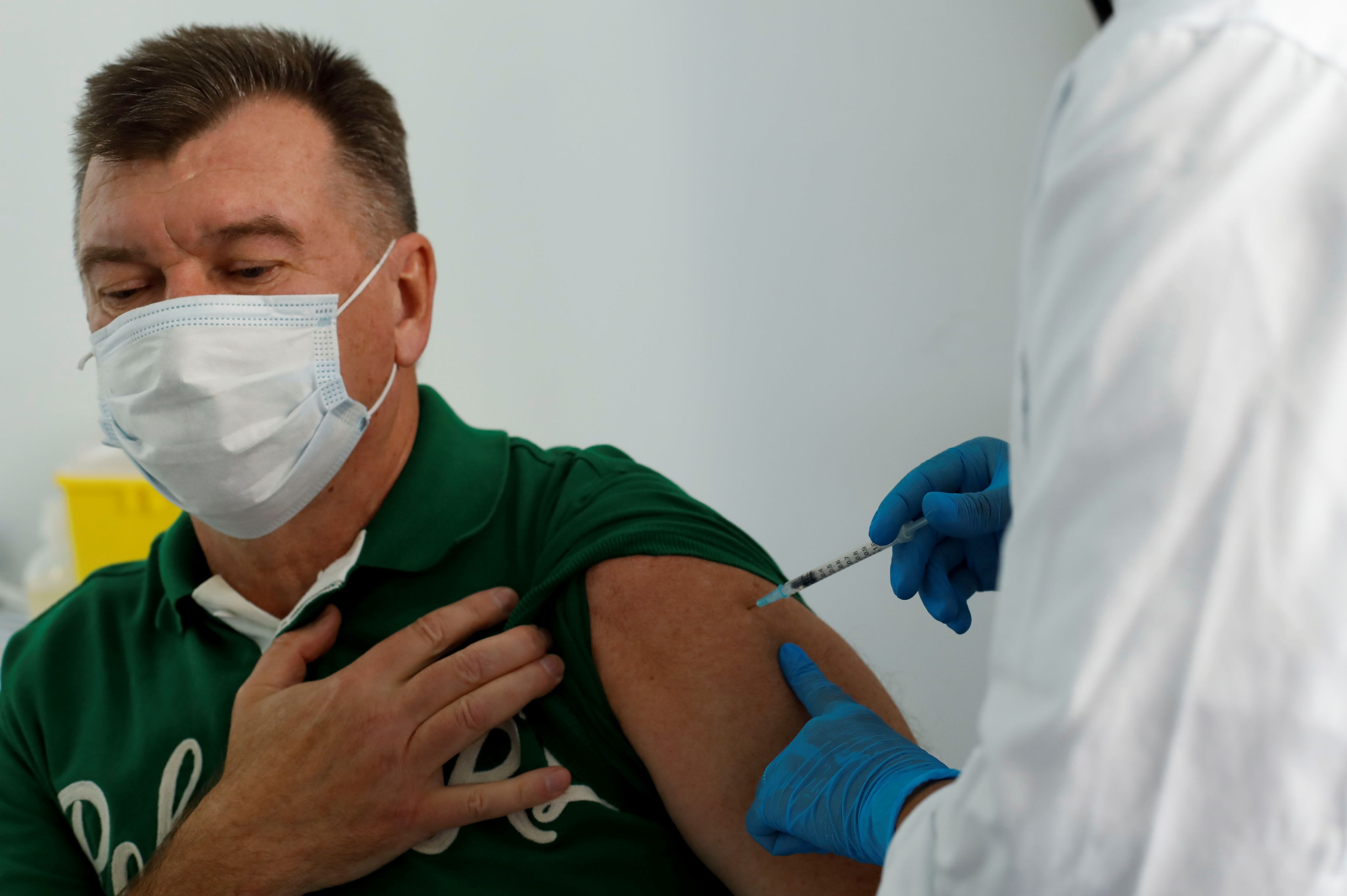
REUTERS/Eva Manez
- Novavax ha afirmado este jueves que su vacuna contra el coronavirus tiene un 89% de efectividad en la prevención de casos de COVID-19, según los resultados de su ensayo clínico en Reino Unido.
- En otro ensayo, realizado en Sudáfrica, la vacuna fue mucho menos efectiva, probablemente debido a la variante del coronavirus que surgió allí.
- Descubre más historias en Business Insider España.
La vacuna experimental contra el coronavirus desarrollada por la compañía de biotecnología Novavax ha resultado muy efectiva para prevenir el COVID-19 en un ensayo clínico que ha contado con 15.000 voluntarios británicos, lo que supone una importante validación de una de las principales candidatas a vacuna contra el coronavirus, según ha informado la propia compañía durante esta pasada madrugada.
A pesar del éxito en Reino Unido, los resultados más débiles de un estudio clínico más pequeño realizado en Sudáfrica muestran una clara advertencia del potencial de las variantes del virus para eludir los esfuerzos por derrotarlas.
La vacuna de Novavax fue un 49% efectiva en la prevención de la enfermedad en el ensayo de Sudáfrica, donde 9 de cada 10 casos fueron causados por una cepa viral preocupante llamada B.1.351. El jueves, Estados Unidos confirmó los primeros casos de esa cepa. También en nuestro país, donde el Servicio Gallego de Salud (Sergas) detectó el jueves la presencia de esta variante en un hombre de 30 años vinculado a la industria naval.
La variante sudafricana de COVID-19 podría reducir la eficacia de la vacuna a la mitad
La compañía publicó los resultados del ensayo en un comunicado de prensa y aseguró que planea enviarlos a una revista científica para su revisión por pares.
Las acciones de Novavax subieron un 30% en las negociaciones posteriores al cierre de mercado. Con todo, el éxito del ensayo clínico llevado a cabo en Reino Unido culmina una ardua historia de investigación de vacunas de tres décadas para la empresa, que nunca ha desarrollado un medicamento comercial hasta la fecha.
Los estudios del Reino Unido y Sudáfrica todavía están en curso, y el anuncio del jueves detalla los resultados provisionales de ambos ensayos. Eso significa que es probable que cambie la eficacia real de la vacuna a medida que se registren más infecciones en las investigaciones.
Los resultados del estudio de Sudáfrica son un hallazgo preocupante, pero ya conocido
La variante, B.1.351, se descubrió por primera vez en diciembre en Sudáfrica y desde entonces se ha extendido a al menos 30 países.
Cuando el estudio de Novavax comenzó a contabilizar los casos de COVID-19 entre los voluntarios, B.1.351 ya era la cepa dominante en Sudáfrica y representaba aproximadamente el 80% de los casos, según los datos de Nextstrain.org presentados por Novavax.
El hallazgo clave del estudio es que la vacuna tuvo una efectividad del 49% en Sudáfrica. El ensayo registró 44 casos de COVID-19, 15 entre los voluntarios que recibieron inyecciones de Novavax y 29 del grupo placebo.
Son en cualquier caso datos más limitados que los ensayos clínicos realizados por Pfizer y Moderna, que respectivamente registraron más de 150 casos.
Aún así, el estudio de 4.406 personas proporciona la evidencia más sólida hasta la fecha de que las vacunas pueden ser menos efectivas contra ciertas variantes del virus, particularmente B.1.351.
Dado el pequeño número de casos, la eficacia real de la vacuna en Sudáfrica podría variar enormemente. El análisis preliminar ha determinado una probabilidad del 95% de que las dosis tengan entre un 6% y un 73% de efectividad.
La preocupación es evidente y ha forzado ya un cambio en la estrategia de Novavax. La compañía comenzará a investigar una nueva versión de su vacuna que incluya específicamente la variante B.1.351, con el objetivo de comenzar las pruebas en humanos en el segundo trimestre de 2021.
Algunas investigaciones preliminares ya plantearon preocupaciones similares esta semana sobre que otras vacunas contra el coronavirus pueden no funcionar tan bien contra esta variante. La vacuna de Moderna, por ejemplo, mostró una reducción de más de seis puntos en los anticuerpos neutralizantes, las proteínas que matan el virus en el corazón de la respuesta inmune, cuando se expuso a B.1.351.
Tanto Moderna como Pfizer han dicho que esperan que sus dosis funcionen contra la nueva variante. Pero ambas también han comenzado a desarrollar vacunas específicas frente a las variantes por precaución.
Incluso si tiene éxito, es probable que Novavax esté todavía a meses de comenzar a vacunar a la gente
Una vacuna eficaz de Novavax sería una buena aportación al arsenal mundial de herramientas para combatir la pandemia, que ha infectado a más de 100 millones de personas.
Los reguladores occidentales han autorizado hasta ahora vacunas de Pfizer-BioNTech, AstraZeneca-Oxford y Moderna, y varios otros también han obtenido la aprobación, pero los suministros siguen siendo muy limitados.
Novavax ha comentado que para mediados de 2021 su objetivo es poder producir a un ritmo de 2.000 millones de dosis por año, aunque no está claro cuántas podría distribuir este año.
A pesar del éxito clínico en Reino Unido, el director ejecutivo de Novavax, Stanley Erck, ha explicado que probablemente la compañía tardaría dos o tres meses en solicitar una autorización de emergencia ante los reguladores de ese país.
El gobierno de EEUU llegó a un acuerdo de financiación de 1.600 millones de dólares con Novavax el año pasado, dando prioridad a su candidata a vacuna para pruebas a gran escala en dicho país y en México. Ese estudio de 30.000 personas ha inscrito hasta ahora a más de 16.000 voluntarios. La empresa espera finalizar la inscripción a mediados de febrero.
Aquí, la Comisión Europea está cerrando un acuerdo de compra con la farmacéutica para asegurarse la reserva de 100 millones de dosis, con la posibilidad de adquirir posteriormente hasta 100 millones de dosis más.
Otros artículos interesantes:
Conoce cómo trabajamos en Business Insider.