La vacuna de Pfizer será aprobada para su administración en adolescentes a finales de mayo, según la Agencia Europea del Medicamento
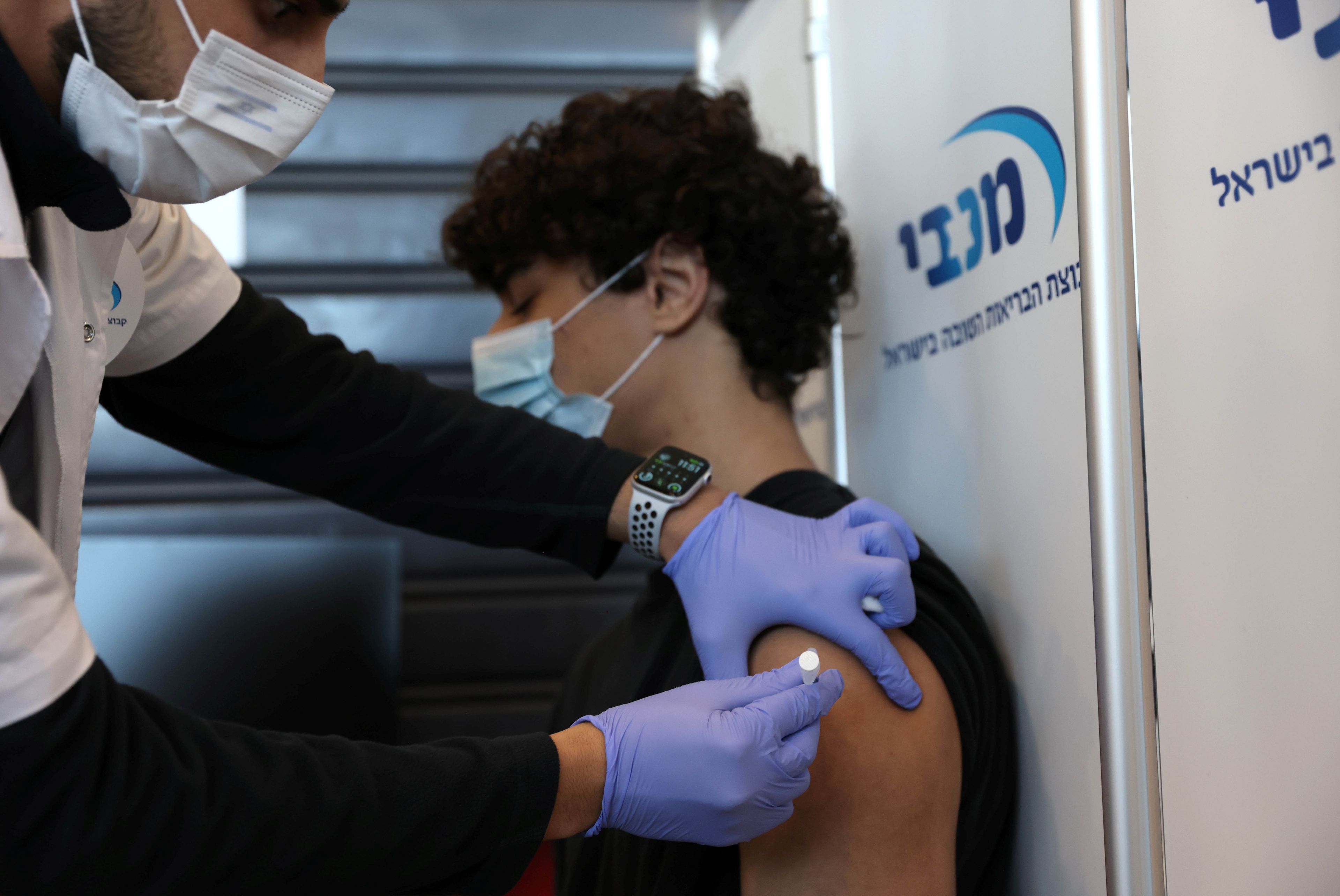
Reuters
- La Agencia Europea del Medicamento (EMA) fija la fecha para su veredicto, después de que Estados Unidos haya autorizado la vacuna en mayores de 12 años.
- Según ha explicado Emer Cooke, la directora de la entidad, se ha solicitado a Pfizer los resultado de los últimos estudios realizado en el país norteamericano para adelantar el proceso, que estaba previsto para el mes de junio.
- Descubre más historias en Business Insider España.
La Agencia Europea del Medicamento (EMA) se encuentra inmersa desde el pasado 30 de abril en un proceso de revisión de los datos recabados por Pfizer en sus ensayos clínicos sobre el uso de la vacuna entre adolescentes.
Si el veredicto es positivo, el organismo regulador prevé dar luz verde en las próximas 3 semanas para que los menores, de entre 12 y 15 años de edad, se sumen a las campañas de vacunación en el viejo continente.
Emer Cooke, directora de la entidad, ha explicado que tenían previsto ofrecer sus resultados ya entrado el mes de junio, pero que han solicitado a la farmacéutica estadounidense que aporte toda la documentación que tenga sobre las pruebas con voluntarios para intentar resolver cuanto antes el proceso, a finales de mayo.
“Nos han prometido datos de los ensayos clínicos en las próximas 2 semanas y vamos a acelerar la revisión”, ha afirmado en una entrevista conjunta ofrecida a 4 medios europeos, entre ellos El Mundo.
La falta de voluntarios adolescentes en ensayos
La vacunación de los adolescentes ha estado desde el inicio de la pandemia en el foco de la lupa de los investigadores. La ausencia de voluntarios de esas franjas demográficas en los ensayos masivos que las farmacéuticas llevaron a cabo en 2020 les ha dejado fuera de los actuales planes de vacunación.
Por eso, hasta la fecha solo estaba contemplado que los 27 estados miembros del bloque inocularan sus dosis sobre la población mayor de 16 años; sin embargo, las farmacéuticas han abierto nuevas vías de investigación para subsanar este problema.
Uno de los creadores de la vacuna de Pfizer pone fecha al fin de la pandemia
La voluntad de la EMA para autorizar el uso de la vacuna de Pfizer en los adolescentes confirma las preferencias de Bruselas con la compañía estadounidense. La Comisión Europea ya firmó esta semana un nuevo contrato para el envío de 1.800 millones de dosis adicionales en los próximos 3 años. El objetivo era precisamente contar con suministros para la protección de los menores de 16 años, así como para una posible vacunación de refuerzo.
En todo caso, se trata de un plan a medio plazo. Por el momento, la mayor parte de los países europeos se encuentran enfrascados en la inmunización de colectivos más mayores. En España, por ejemplo, esta semana se han iniciado las inyecciones sobre el grupo de 50 a 59 años de edad, que representa a más de 7 millones de ciudadanos, por lo que la entrada de los adolescentes en la cadena de prioridad se antoja todavía lejana.
Europa sigue el camino marcado por Estados Unidos
La EMA ha acelerado su revisión para no volver a quedarse por detrás de los planes de las grandes potencias mundiales. Estados Unidos ya acordó este martes la autorización para el uso de emergencia de la vacuna de Pfizer en las personas mayores de 12 años.
La Administración de Fármacos y Alimentos (FDA) del país norteamericano dio por buenos los ensayos de la farmacéutica con varias semanas de ventaja sobre Europa. Un fenómeno habitual que ya ha ocurrido con la aprobación del resto de vacunas del mercado, ya que las revisiones del regulador europeo suelen demorarse más en el tiempo.
Janet Woodcock, doctora y comisionada en funciones de la FDA, explicó que el veredicto representa un importante avance en la lucha contra el coronavirus para proteger también a la población más joven y acercar al país hacia el final de la crisis sanitaria.
“Padres y tutores pueden estar seguros de que la agencia llevó a cabo una revisión rigurosa y exhaustiva de todos los datos disponibles”, apuntó.
El próximo reto: los niños de 6 a 11 años
El siguiente paso en la carrera científica de la vacuna pasa por garantizar que la vacuna también sea efectiva y segura para los niños de entre 6 y 11 años de edad. Pfizer ya ha iniciado los ensayos clínicos sobre este sector demográfico, con el objetivo de ampliar el alcance de su fármaco en el futuro.
Aunque se trata de un grupo de población que tiene muy pocas posibilidades de sufrir un caso grave de coronavirus, su vacunación sigue siendo un punto clave para controlar el avance de la enfermedad. En Estados Unidos, un 20% de la población son niños.
Artículo original deEconomía Digital

Otros artículos interesantes:
Conoce cómo trabajamos en Business Insider.