La Unión Europea podría autorizar pronto la venta del remdesivir como tratamiento efectivo contra el COVID-19
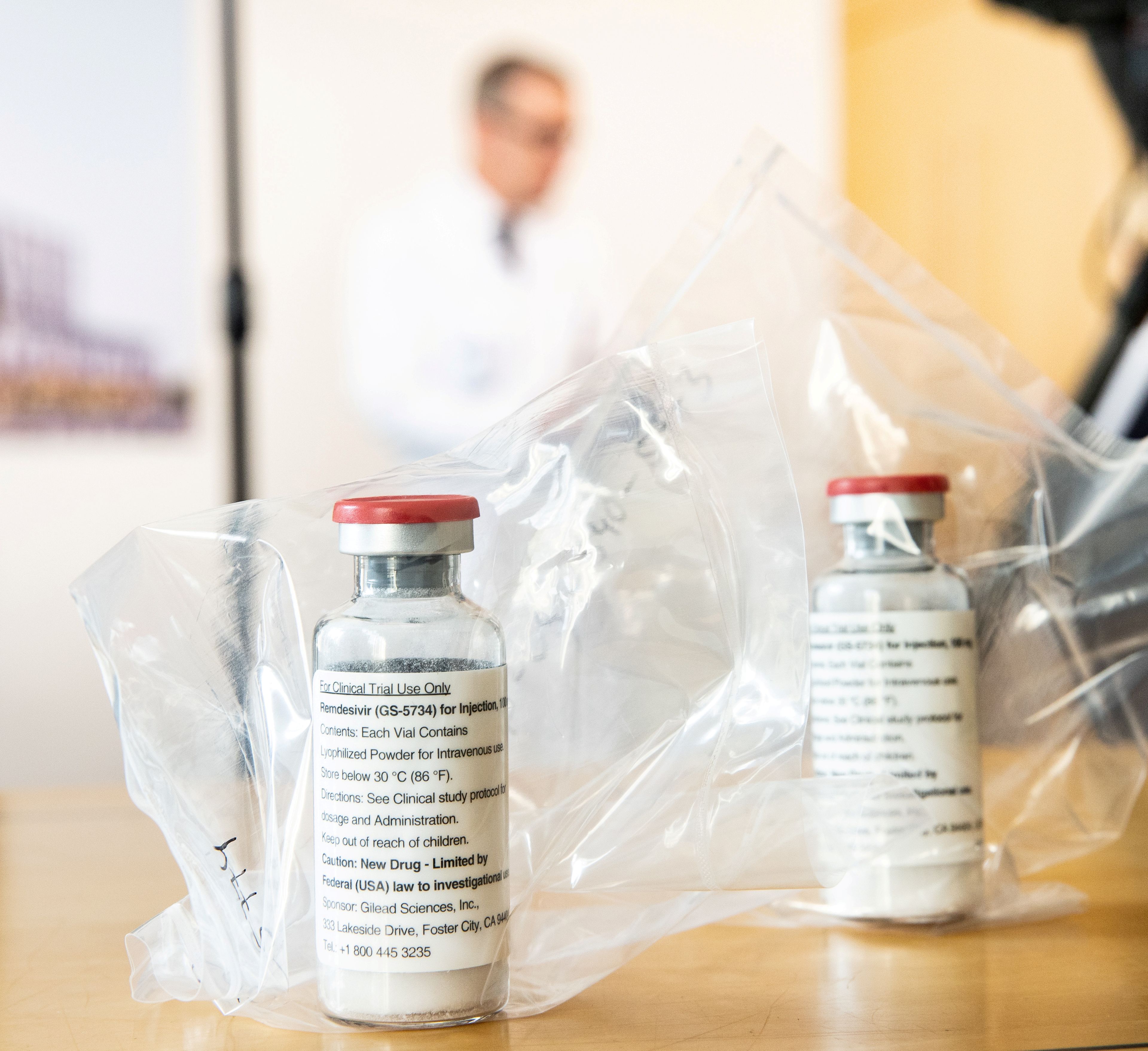
- La UE podría dar luz verde en los próximos días a la comercialización del remdesivir para su uso contra el COVID-19.
- "Podría ser que una autorización condicional de comercialización pueda ser emitida en los próximos días", ha dicho el director ejecutivo de la Agencia Europea de Medicamentos, Guido Rasi, en el Parlamento de la UE en Bruselas.
- La Agencia Europea de Medicamentos (EMA) ya ha recomendado el uso compasivo de remdesivir, pero la autorización permitiría su venta durante un año a los 27 países de la UE.
- Estas autorizaciones permiten comercializar un fármaco para el que no se tienen todos los datos cuando están "destinados a situaciones de emergencia en respuesta a amenazas para la salud pública reconocidas por la Organización Mundial de la Salud".
- Descubre más historias en Business Insider España.

La Unión Europea podría dar luz verde en los próximos días a la venta del fármaco remdesivir como tratamiento eficaz contra el COVID-19, según informa The Guardian.
"Podría ser que una autorización condicional de comercialización pueda ser emitida en los próximos días", ha dicho el director ejecutivo de la Agencia Europea de Medicamentos, Guido Rasi, en el Parlamento de la UE en Bruselas.
La Agencia Europea de Medicamentos (EMA) ya ha recomendado el uso compasivo de remdesivir, que permite que un medicamento sea administrado a los pacientes incluso antes de que su venta haya sido autorizada.
En España, el remdesivir se utiliza en los hospitales para tratar a pacientes como parte del ensayo clínico global SOLIDARITY lanzado por la Organización Mundial de la Salud y también está autorizado su uso compasivo.
A mediados de abril empezaron a publicarse las primeras confirmaciones de que el fármaco era eficaz contra el coronavirus, acelerando la recuperación de los pacientes.
Sin embargo, la autorización condicional de comercialización de la UE daría un paso más, ya que permite que un medicamento se venda durante un año en el bloque de los 27 países antes de que se disponga de todos los datos necesarios sobre su eficacia y efectos secundarios, según informa Reuters.
Según la legislación, la autorización basada en datos menos completos de lo habitual se puede conceder "para satisfacer necesidades no cubiertas de los pacientes y en interés de la salud pública" para medicamentos "destinados al tratamiento, la prevención o el diagnóstico de enfermedades gravemente debilitantes o potencialmente mortales, o bien medicamentos destinados a situaciones de emergencia en respuesta a amenazas para la salud pública reconocidas por la Organización Mundial de la Salud".
Gilead, la biotecnológica detrás del prometedor tratamiento, ya ha firmado acuerdos de licencia voluntaria con 5 fabricantes de medicamentos genéricos para reforzar la oferta del remdesivir en 127 países.
Desde el primer momento, la Organización Mundial de la Salud mostró sus esperanzas para el medicamento. A finales de febrero, cuando Gilead comenzaba los ensayos clínicos con el remdesivir, Bruce Aylward, subdirector general de la Organización Mundial de la Salud, declaró: "En este momento, solo hay un medicamento que creemos que puede tener una eficacia real y ese es el remdesivir".
Conoce cómo trabajamos en BusinessInsider.
Etiquetas: Unión EuropeaEnfermedades, Salud, España, Ciencia, Coronavirus