Gilead ha construido un gigante de la biotecnología tratando virus como el VIH y la hepatitis C y ahora podría ganar miles de millones con el primer tratamiento eficaz contra el coronavirus

- Gilead Sciences es una farmacéutica con más de 30 años de historia y responsable de uno de los tratamientos más prometedores para el coronavirus.
- La compañía tiene una larga historia de desarrollo y comercialización de tratamientos para enfermedades virales como el VIH, la hepatitis C, y ahora el coronavirus.
- A menudo es criticada por los precios de sus medicamentos.
- El 29 de junio, Gilead dijo que el precio de remdesivir será de hasta unos 2.090 euros por tratamiento, o hasta 348 euros por vial.
- Así es como Gilead ha pasado de ser una startup a una de las compañías antivirales más formidables en la carrera por tratar el novedoso coronavirus.
- Descubre más historias en Business Insider España.
Mientras el mundo busca una forma de prevenir y tratar el nuevo coronavirus, una farmacéutica con 33 años de historia es la responsable de uno de los tratamientos más prometedores hasta el momento.
El tratamiento, remdesivir, es un fármaco antiviral hecho por Gilead Sciences que fue desarrollado inicialmente para tratar el Ébola hace una década.
Un estudio sobre la eficacia del remdesivir en el tratamiento de pacientes hospitalizados con coronavirus, publicado en mayo, demostró que los pacientes que recibieron el medicamento se recuperaron más rápidamente. Sin embargo, no mostró una marcada reducción de las muertes.
Los resultados fueron la base de la decisión de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) de permitir el uso de emergencia del fármaco en pacientes hospitalizados con COVID-19, la enfermedad causada por el nuevo coronavirus. A partir de agosto, Gilead explorará cómo podría funcionar el fármaco si es inhalado, con la esperanza de que esté más disponible para los pacientes que en su forma intravenosa.
Remdesivir está lejos de ser la primera incursión de Gilead en los medicamentos antivirales. Desde la década de 1990, la compañía tiene una larga historia de desarrollo y venta de tratamientos para el VIH, así como para infecciones como la hepatitis B y C. La compañía obtuvo 22.400 millones de dólares en ventas en 2019, la mayoría de los cuales provinieron de las ventas de sus tratamientos antivirales.
Gilead está donando sus reservas de remdesivir para su distribución bajo la autorización de uso de emergencia de la FDA, pero la pregunta de cuánto podría cobrar el fabricante de medicamentos por su tratamiento contra el coronavirus era objeto de debate. De acuerdo con el Instituto de Revisión Clínica y Económica, un organismo de control de la industria sin ánimo de lucro, un precio justo sería de hasta 4.500 dólares por paciente (unos 4.005 euros).
El 29 de junio, Gilead anunció que cobrará hasta 3.120 dólares (en torno a 2.700 euros) por un tratamiento de cinco días de remdesivir, cobrando hasta 520 dólares (unos 464 euros) por dosis. La sanidad pública y los gobiernos tendrán un precio reducido de 2.340 dólares (unos 2.090 euros) por cada tratamiento, señaló la compañía.
A ese precio, los analistas de Wall Street esperan que aporte 2.300 millones de dólares a la compañía solo en 2020.
Así es como Gilead pasó de ser una startup a una de las más formidables compañías antivirales en la carrera por tratar el nuevo coronavirus, con un valor de mercado de más de 96.000 millones de dólares.
Gilead vendió su desarrollo de la tecnología antisentido en 1998 a la compañía ahora conocida como Ionis Pharmaceuticals.
Leer más: Los 4 tratamientos contra el coronavirus que la OMS ha puesto en marcha en un ensayo global
En el tiempo transcurrido, la compañía había estado trabajando en tratamientos antivirales, comenzando con la contratación de John Martin en 1990. Antes de unirse a Gilead, Martin trabajó en la compañía farmacéutica Bristol-Myers Squibb, donde dirigió la química antiviral. Martin pasó a ser el CEO de Gilead desde 1996 hasta 2016.
Incluso con algunas aprobaciones en los años 90, no fue hasta 2002 cuando Gilead alcanzó la rentabilidad, 15 años después de su fundación.
Su primera incursión en el tratamiento del VIH y el SIDA no concluyó con éxito. El fármaco, ahora conocida como Hepsera, fue inicialmente rechazada por la FDA, que citó problemas de riñón en pacientes que recibieron altas dosis.
La compañía finalmente logró usar el tratamiento en dosis más bajas para tratar la hepatitis B, una infección del hígado causada por el virus de la hepatitis B. La FDA aprobó el medicamento en 2002.
Para 2004, la FDA había dado su aprobación a Truvada, una combinación de emtricitabina, conocida como Emtriva, y tenofovir, también conocido como Viread. En ese momento, se esperaba que se convirtiera en un medicamento de gran éxito, tras el éxito comercial de Viread, que en ese momento era el fármaco para el SIDA más vendido en Estados Unidos, informó The Mercury News en un artículo de 2004 sobre el cambio de la empresa.
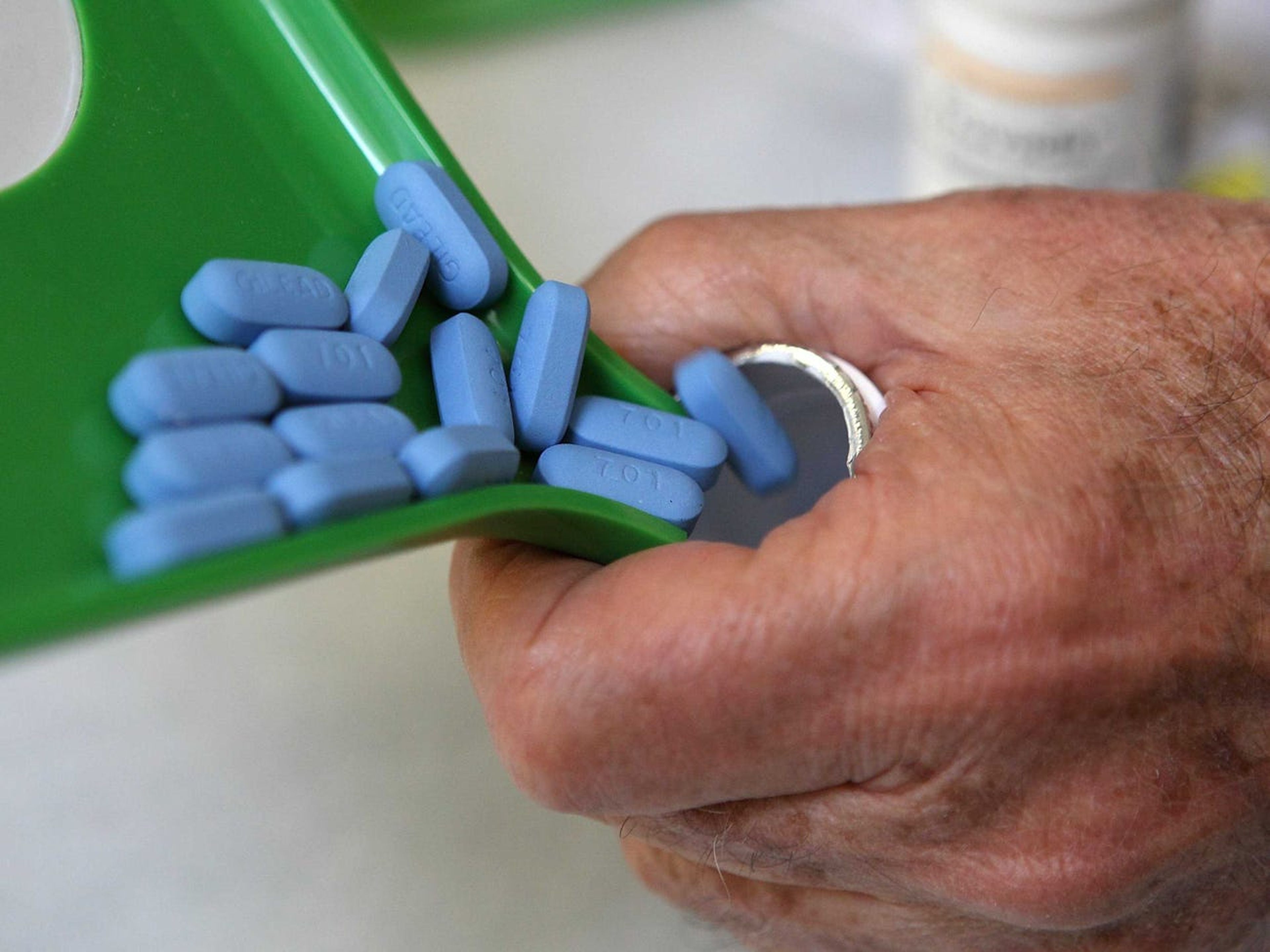
El éxito de Gilead en el VIH
En los 15 años desde la aprobación de Truvada, Gilead se ha convertido en una potencia antiviral. Su portfolio de medicamentos para el VIH generó 16.400 millones de dólares en ventas en 2019.
En ese tiempo, Gilead pasó de solo tratar el VIH a demostrar que también podía prevenirlo.
Con la aprobación de Truvada para la prevención del VIH en 2012, las personas en riesgo de infección por VIH obtuvieron una nueva e importante herramienta para protegerse.
Los medicamentos se conocen como PrEP, o profilaxis preexposición. Son una gran parte del plan de la administración Trump para disminuir masivamente los nuevos casos de VIH en Estados Unidos para el 2030.
Aún así, Estados Unidos han tenido dificultades para hacer llegar los medicamentos a todas las personas que los necesitan y para proporcionar la atención adecuada a las personas con VIH, por lo que la tasa de nuevas infecciones se mantuvo relativamente estable de 2012 a 2016.
Sin seguro, el precio medio de venta al público para 30 días de Truvada es de 2.200 dólares (unos 1.950 euros), según GoodRx.
Algunos planes de seguros cubren el fármaco, y la mayoría de los planes de salud deberán cubrirlo a partir del próximo año.
La administración Trump demandó en noviembre a Gilead, buscando daños vinculados a las patentes del Departamento de Salud y Servicios Humanos relacionadas con la prevención del VIH.

La píldora de Gilead para la hepatitis C de 1.000 dólares
El escrutinio sobre cuánto cobra Gilead por sus tratamientos antivirales llegó a su punto máximo en 2013, cuando la compañía obtuvo la aprobación de su tratamiento contra la hepatitis C, Sovaldi.
Gilead obtuvo el medicamento en su adquisición de 11.000 millones de dólares de Pharmasset en 2011.
En diciembre de 2013, la FDA aprobó Sovaldi, un tratamiento de 12 semanas para la hepatitis C cuyo precio se fijó a 1.000 dólares por píldora, o 84.000 dólares por el tratamiento completo. Pero en el otro extremo había una alta tasa de éxito de los pacientes curados de la infección.
Comercialmente, el fármaco fue un gran éxito para Gilead. Forbes en 2015 lo consideró como uno de los lanzamientos más exitosos de la historia, citando su capacidad de lograr 10.000 millones de dólares en ventas durante su primer año.
La aprobación fue un momento crucial para el debate sobre los precios de los medicamentos, con las organizaciones encargadas de cubrir el alto coste del fármaco dando marcha atrás. Los miembros del Comité de Finanzas del Senado lanzaron una investigación sobre el precio, concluyendo en 2015 que la compañía puso las ganancias por delante de los pacientes.
Como los rivales lanzaron sus propios fármacos para la hepatitis C, los precios y las ventas de Gilead bajaron rápidamente. En su punto máximo, Gilead ganó 19.100 millones de dólares en 2015 con sus medicamentos contra la hepatitis C. En 2019, la compañía ganó solo 2.900 millones de dólares y lo atribuyó a un precio de venta promedio más bajo.
Con el dinero de su éxito en los tratamientos de la hepatitis C, Gilead se tomó su tiempo antes de adquirir el fabricante de medicamentos contra el cáncer Kite en 2017 por 12.000 millones de dólares. El movimiento se produjo pocos meses antes de la aprobación del primer tratamiento de Kite, Yescarta, uno de una clase de tratamientos altamente personalizados contra el cáncer con terapias de Células CART.
En 2016, Martin dejó el puesto de CEO, y el directivo John Milligan tomó su lugar antes de retirarse en 2019.
O'Day es el CEO de Gilead desde marzo de 2019, y se unió después de un período de 31 años en el gigante farmacéutico Roche. Su contratación dio lugar a que los analistas esperaran que O'Day marcara el comienzo de un período de negociaciones para reponer la cartera de medicamentos de la empresa.
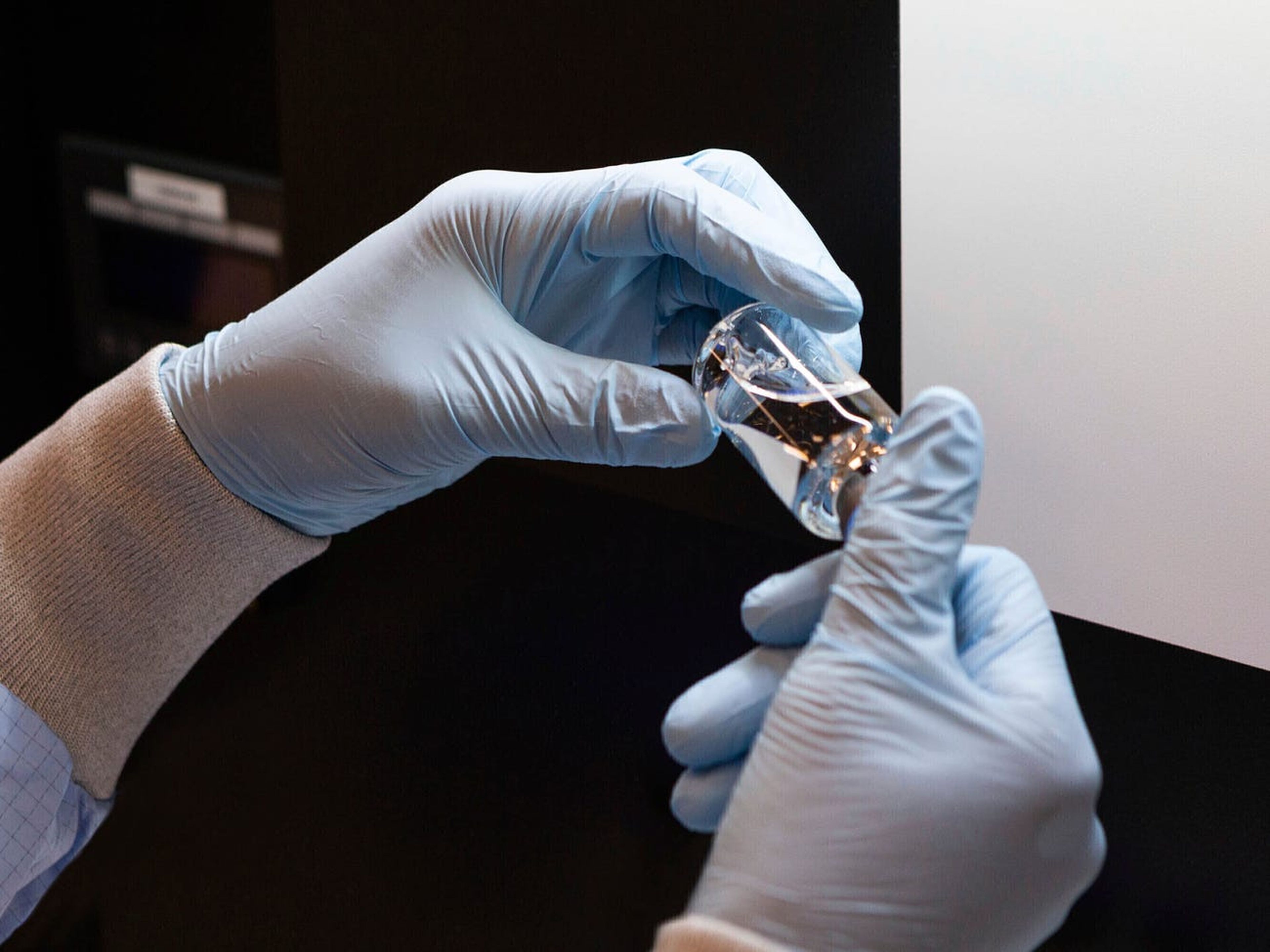
La era del remdesivir
Luego vino la pandemia de coronavirus.
Para tratar el COVID-19, los investigadores están probando todo, desde medicamentos antipalúdicos a antivirales, e incluso medicamentos comunes para la acidez estomacal, con la esperanza de que más pacientes sobrevivan a las formas graves de la enfermedad y se recuperen más rápido. Algunos están buscando formas de usar el propio cuerpo de los pacientes para combatir el virus con tratamientos de anticuerpos. También se están realizando esfuerzos para desarrollar vacunas de uso preventivo.
Al principio de la pandemia, los investigadores y los médicos consideraron cómo podría funcionar remdesivir, un medicamento desarrollado como tratamiento para el Ébola.
Se había desarrollado como parte de un esfuerzo por encontrar tratamientos para la hepatitis C y el virus sincitial respiratorio, dijo un portavoz de Gilead a Business Insider en abril.
Los resultados publicados en 2017 encontraron que el medicamento mostraba actividad contra los coronavirus responsables de dos brotes importantes: SARS y MERS. También se había utilizado en estudios durante la epidemia del virus del Ébola en África occidental entre 2013 y 2016 y posteriormente se le dio autorización de uso de emergencia para tratar el Ébola como parte de la epidemia en el Congo.
El fármaco fue uno de los cuatro estudiados para el Ébola como parte de un ensayo aleatorio publicado en 2019, pero otros dos fármacos superaron al remdesivir.
Pero debido a que ya había sido probado en pacientes, el medicamento había demostrado ser seguro para que los humanos lo tomaran cuando se trataba de tratar a pacientes con COVID-19.
Cuando el primer caso de COVID-19 en Estados Unidos apareció en el estado de Washington en enero, los profesionales médicos que atendían al paciente decidieron administrar remdesivir en el séptimo día del hombre en el hospital, según un informe de caso publicado en el New England Journal of Medicine. El paciente finalmente se recuperó.
En febrero, un funcionario de la Organización Mundial de la Salud dijo que el remdesivir era "un medicamento que en este momento creemos que puede ser eficaz" para el tratamiento de COVID-19. Las acciones de Gilead alcanzaron un máximo de 16 meses ese día. A fines de febrero, Gilead había iniciado ensayos del medicamento en los países asiáticos donde el virus se estaba propagando y en Estados Unidos.
A lo largo de abril, se fueron filtrando datos "esperanzadores" sobre el tratamiento y su eficacia en pacientes hospitalizados. Eso culminó en que los Institutos Nacionales de Salud dieron a conocer datos preliminares a finales de ese mes que mostraban que los pacientes que tomaban remdesivir se recuperaban un 31% más rápido que los que recibían el medicamento placebo. El viernes se publicaron datos más completos.
El 1 de mayo, la FDA emitió una autorización de emergencia para el uso del medicamento. Aunque no es una aprobación, podría permitir que más pacientes hospitalizados recibieran el medicamento. Por ahora, el fármaco está autorizado para ser administrada a pacientes hospitalizados severamente enfermos a través de una infusión intravenosa en el curso de un período de cinco o diez días.
Pero los suministros son limitados. La fabricación del fármaco es un proceso largo, y Gilead anticipa que fabricará más de un millón de tratamientos para finales de 2020, invirtiendo 1.000 millones de dólares para aumentar la fabricación. Ahora que Gilead ha fijado un precio para el remdesivir de hasta 3.120 dólares por tratamiento, puede pasar de donar el medicamento a hacer negocio con él.
La realidad es que el remdesivir no ayudará a muchos pacientes con coronavirus, y todavía se necesitan otros tratamientos. Los investigadores ya están probando el usar el remdesivir en combinación con otros medicamentos para hacerlo más potente.
También se están haciendo esfuerzos para hacer tratamientos usando el propio cuerpo de los pacientes para combatir el virus con anticuerpos, aunque tardarán un poco más en desarrollarse. Las farmacéuticas esperan tener los tratamientos disponibles para el otoño.
De startup a una compañía con un fármaco de éxito contra el SIDA
Como muchas startups, Gilead fue inicialmente financiada por inversores de riesgo. La compañía, fundada en 1987 por el Dr. Michael Riordan, fue respaldada por compañías de capital de riesgo, incluyendo Menlo Ventures. Riordan pasó un año en Menlo antes de iniciar Gilead. El nombre de la compañía es una referencia bíblica al bálsamo de Gilead, un tratamiento usado medicinalmente.
En enero de 1992, la empresa de Foster City, California, hizo su debut en la bolsa, recaudando 86,25 millones de dólares en el proceso.
Inicialmente, la compañía se centró en la tecnología antisentido, tratamientos construidos con la intención de inactivar los genes en el cuerpo que producen proteínas que causan enfermedades. Pero en los años 90, la compañía se dio cuenta de que la tecnología iba a llevar algún tiempo.
"Nos dimos cuenta bastante rápido de que esto iba a ser muy difícil", dijo Norbert Bischofberger, el jefe de investigación y desarrollo de Gilead durante mucho tiempo, al San Francisco Chronicle en 2003.
Otros artículos interesantes:
Conoce cómo trabajamos en Business Insider.