10 razones para convencer a un amigo escéptico de ponerse la vacuna
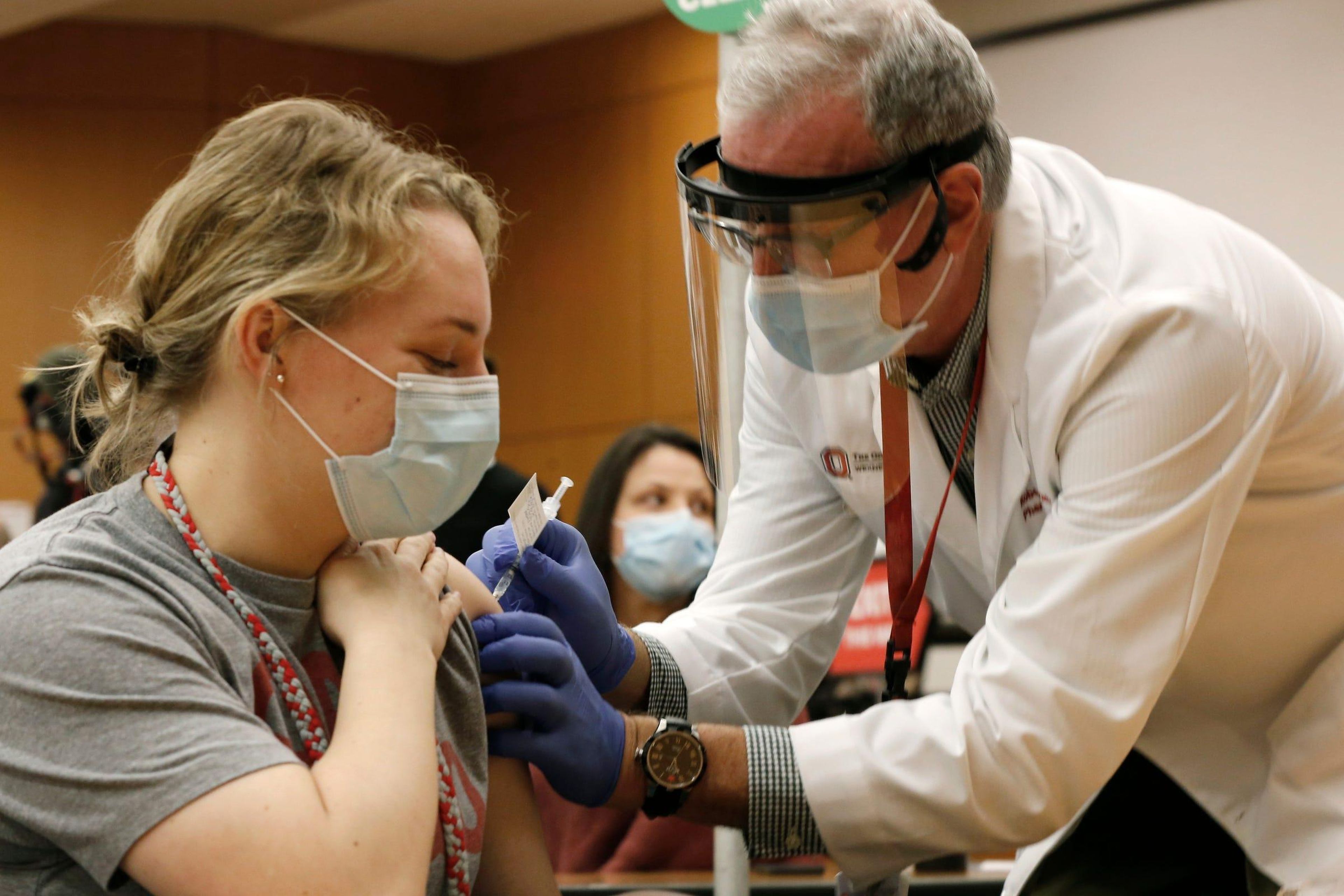
- La Agencia Europea del Medicamento (EMA) y la norteamericana FDA, han aprobado el uso de emergencia de 2 vacunas contra COVID-19.
- Ninguna de las 2 candidatas ha planteado graves problemas de seguridad en los grandes ensayos clínicos, con diversos grupos de voluntarios en los que se han puesto a prueba.
- Aquí tienes 10 razones para confiar en la seguridad de las vacunas y convencer a los amigos más escépticos.
- Descubre más historias en Business Insider España.

En España, se han administrado unas 406.091 dosis iniciales de la vacuna contra el coronavirus de Pfizer, de las 743.925 entregadas, desde su llegada el pasado 27 de diciembre hasta el 11 de enero, acorde al último informe del Ministerio de Sanidad.
A partir del 21 de enero, la candidata de Moderna se sumará a primera campaña de vacunación y se distribuirá por todo el territorio.
Ambas, han sido autorizadas por la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) y la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), lo que indica que son lo suficientemente seguras como para evitar casos de COVID-19 sin poner en riesgo la vida de los pacientes.
Pero, a principios de diciembre, sólo 1 de cada 3 españoles se vacunaría contra COVID-19 "inmediatamente", conforme a los datos del Centro de Investigaciones Sociológicas.
Un 55% prefiere esperar a conocer los efectos de la candidata y un 60% cambiaría de opinión si su médico se la recomendase.
Sin embargo, en lo que respecta a la seguridad de estas vacunas, ya hay muy buenas razones para confiar en su eficacia.
Estas 10 explicaciones podrían ayudarte a demostrarle a un escéptico la verdad sobre las vacunas contra COVID-19.
La autorización de la EMA y la FDA significa que los científicos expertos están de acuerdo en que los beneficios de las vacunas superan los riesgos
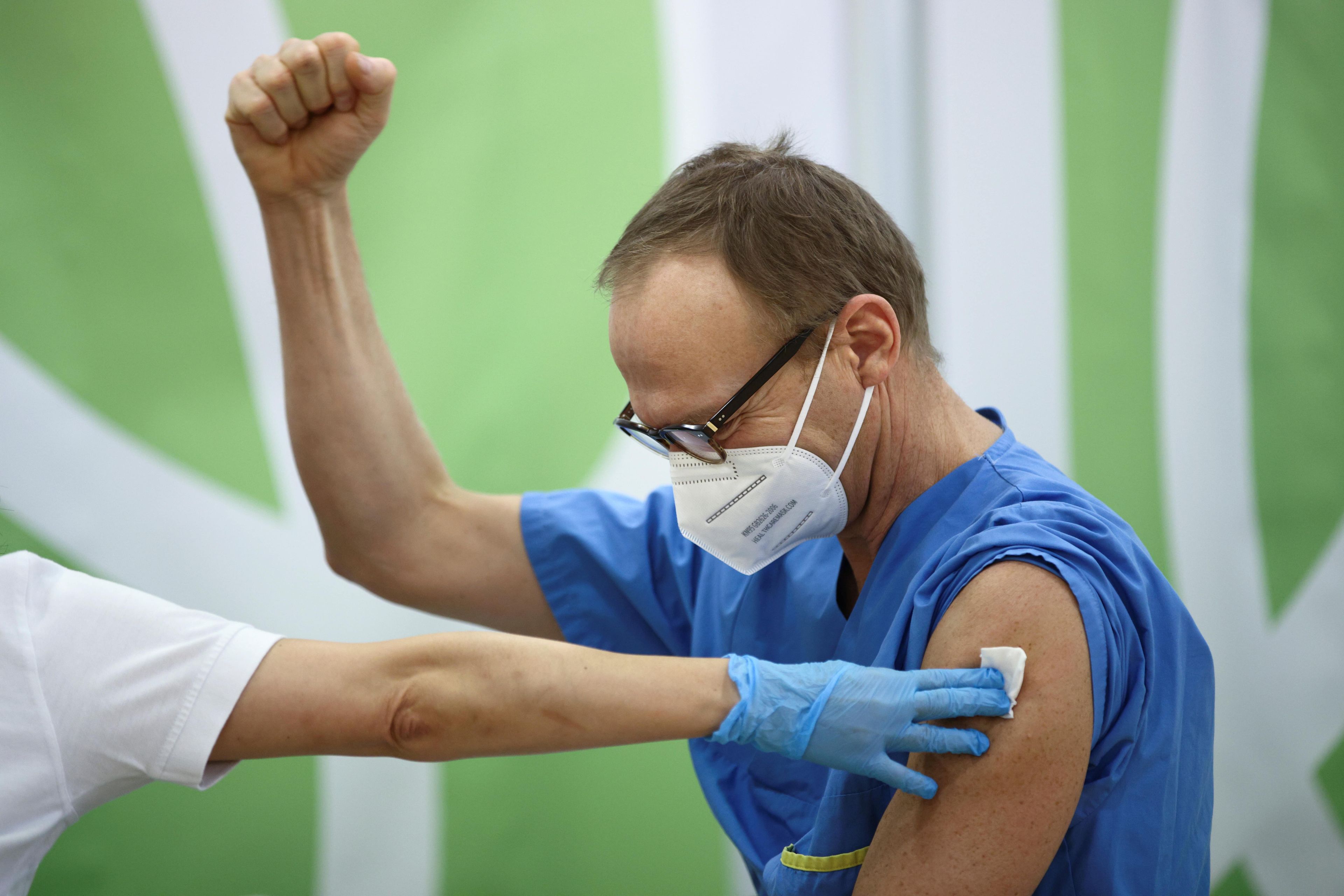
REUTERS/Lisi Niesner
La decisión de la EMA y la FDA, de autorizar las vacunas de Pfizer-BioNTech y Moderna, se basa en la recomendación de un grupo independiente de expertos científicos, que analizó meses de datos de ensayos clínicos en fase avanzada.
Este proceso es estándar para cualquier vacuna, incluyendo las vacunas contra la gripe que se administran cada año.
Al examinar los datos de Pfizer, 17 de los 22 expertos del panel asesor de la FDA estuvieron de acuerdo en que los beneficios de la vacuna "superaban los riesgos de su uso en personas de 16 años o más". Cuatro expertos votaron en contra de esa premisa y un experto se abstuvo.
El CEO de Moderna asegura que su vacuna podría proteger contra el virus durante un par de años
Estos miembros disidentes del comité, en su mayoría, simplemente aclararon que querían más datos de seguridad para las personas de 16 y 17 años. Uno de ellos presionó por al menos 2 meses de datos adicionales que incluyeran más estudios de grupos vulnerables.
Pero ninguno citó grandes preocupaciones de seguridad.
"Habría votado "sí" con más entusiasmo si el lenguaje hubiera sido "... 18 años o más"", reconoció a Business Insider el Dr. David Kim, que dirige la división de vacunas del Departamento de Salud y Servicios Humanos de Estados Unidos.
La vacuna de Moderna recibió un voto de "sí" de 20 de los 21 miembros del comité.
El doctor Michael Kurilla, experto en enfermedades infecciosas de los Institutos Nacionales de Salud, fue el único que se abstuvo en la votación. Asimismo, aclaró que se abstuvo porque la pregunta presentada al panel era demasiado amplia.
Los Gobiernos de todo el mundo podrían haber politizado el proceso de desarrollo de la vacuna, pero eso no afectó a la autorización

Durante el verano, el presidente de Estados Unidos, Donald Trump, sugirió que una vacuna contra el coronavirus podría estardisponible "justo alrededor" de las elecciones del 3 de noviembre. El comentario dio lugar a que muchas personas temiesen que las compañías farmacéuticas se sintieran presionadas para lanzar una vacuna al mercado.
"Me estoy apresurando. Lo estoy haciendo. Estoy presionando a todo el mundo", aseguraba Trump al presentador de radio Geraldo Rivera el 6 de agosto de 2020.
Poco después, las compañías farmacéuticas dieron un paso poco común para calmar la preocupación: en septiembre, 9 de las principales compañías farmacéuticas, incluyendo Pfizer y Moderna, publicaron una declaración conjunta prometiendo anteponer la seguridad a la rapidez.
Las compañías aseguraban "sólo someterse a la aprobación o autorización de uso de emergencia después de demostrar la seguridad y la eficacia a través de un estudio clínico de fase 3 diseñado y realizado para cumplir los requisitos de las autoridades reguladoras expertas como la FDA" —la EMA, en el caso europeo—.
Pfizer también rechazó los fondos del Gobierno de EEUU para la investigación y el desarrollo para evitar posibles conflictos políticos, de acuerdo con las declaraciones recogidas por The New York Times.
Y aunque la FDA requería sólo detectar infecciones en al menos 64 voluntarios en las últimas etapas de los ensayos para evaluar la eficacia de la vacuna, Pfizer esperó a solicitar la autorización hasta que 94 personas se enfermaron.
Las vacunas contra el coronavirus ya han sido probadas en decenas de miles de voluntarios, por lo que los científicos tienen una sólida idea de cómo responde la gente

Los voluntarios del estudio han estado recibiendo inyecciones de Moderna desde marzo y de Pfizer desde abril, tan sólo entre 3 y 4 meses después de la identificación del SARS-CoV-2.
Ambos estudios son ensayos de control aleatorios, lo que significa que los participantes fueron asignados al azar y a ciegas a recibir la vacuna o un placebo.
Tanto el ensayo de Pfizer como el de Moderna tienen un tamaño igual o superior al promedio. Una revisión de 2012 encontró que el ensayo de la vacuna de fase 3 promedio tenía alrededor de 30.000participantes.
El ensayo de última fase de Pfizer involucró a más de 43.000 voluntarios en 6 países y 16 estados de EEUU.
Se registraron 8 casos de COVID-19 en el grupo que recibió la vacuna, en comparación con 162 casos en el grupo de placebo. Eso sugiere que la vacuna es 95% efectiva en la prevención de la enfermedad que el virus provoca, COVID-19.
Por su parte, el ensayo de Moderna involucró a más de 30.000 participantes en 30 estados de EEUU.
Los investigadores identificaron 90 casos de COVID-19 en el grupo de placebo y 5 en el de la vacuna, lo que sugiere que la vacuna es 94.5% efectiva.
La vacuna más efectiva en la historia, la vacuna contra el sarampión, es 97% efectiva.
Moderna y Pfizer y BioNTech diseñaron sus vacunas en pocos días, pero eso no significa que el proceso fuera demasiado rápido

Hasta ahora, la vacuna más rápida que se ha desarrollado, para las paperas, tardó más de 4 años.
Sin embargo, a diferencia de las vacunas tradicionales, las vacunas que dependen del ARN mensajero (ARNm) —material genético que instruye a las células para que produzcan proteínas— pueden ser creadas usando sólo el código genético del virus.
Los científicos chinos secuenciaron y publicaron el genoma del coronavirus en enero.
"No nos estamos saltando pasos. Lo que sucede es que tenemos una mejor tecnología", explicitaba con anterioridad a Business Insider Albert Rizzo, director médico de la Asociación Americana del Pulmón de Estados Unidos.
"¿Por qué se tardó 2 semanas en cruzar el Atlántico en el siglo XIX? Bueno, tuvimos que ir en un barco. Mientras que ahora, puedes cruzar el océano en unas horas".
El cofundador de BioNTech, Ugur Sahin, hizo un diseño aproximado de la vacuna de la compañía durante un fin de semana a mediados de enero, según informó a Business Insider un portavoz de la compañía.
De hecho, en esta misma línea, Moderna desarrolló su vacuna de ARNm en sólo 2 días.
Diferencias entre las vacunas contra el coronavirus: Oxford-AstraZeneca, Pfizer-BioNTech y Moderna
Después, la Operation Warp Speed —asociación encargada de acelerar el desarrollo, la fabricación y la distribución de vacunas— empujó el proceso de Moderna con 483 millones de dólares para desarrollar su vacuna, 472 millones de dólares para avanzar en su ensayo clínico y 1.500 millones de dólares en una orden de compra para 100 millones de dosis.
Mientras, Pfizer invirtió 2.000 millones de dólares de su propio dinero en su iniciativa de vacunas, según The Wall Street Journal.
El laboratorio también probó varias candidatas a la vez, para no tener que volver a la mesa de diseño si alguno no tenía éxito. Y se adelantó meses a su línea de tiempo haciendo ARNm en bolsas desechables en lugar de en tanques de acero.
Como Moderna, Pfizer fabricó dosis de vacunas mientras se realizaban los ensayos clínicos. Además, la compañía optó por almacenar múltiples dosis en un solo frasco y enviarlas a temperaturas subárticas garantizadas para preservar la vacuna, en vez de probar si las dosis podían sobrevivir a temperaturas más altas.
Las vacunas que utilizan la tecnología de ARNm son relativamente nuevas, pero los científicos han estado desarrollando este método durante décadas
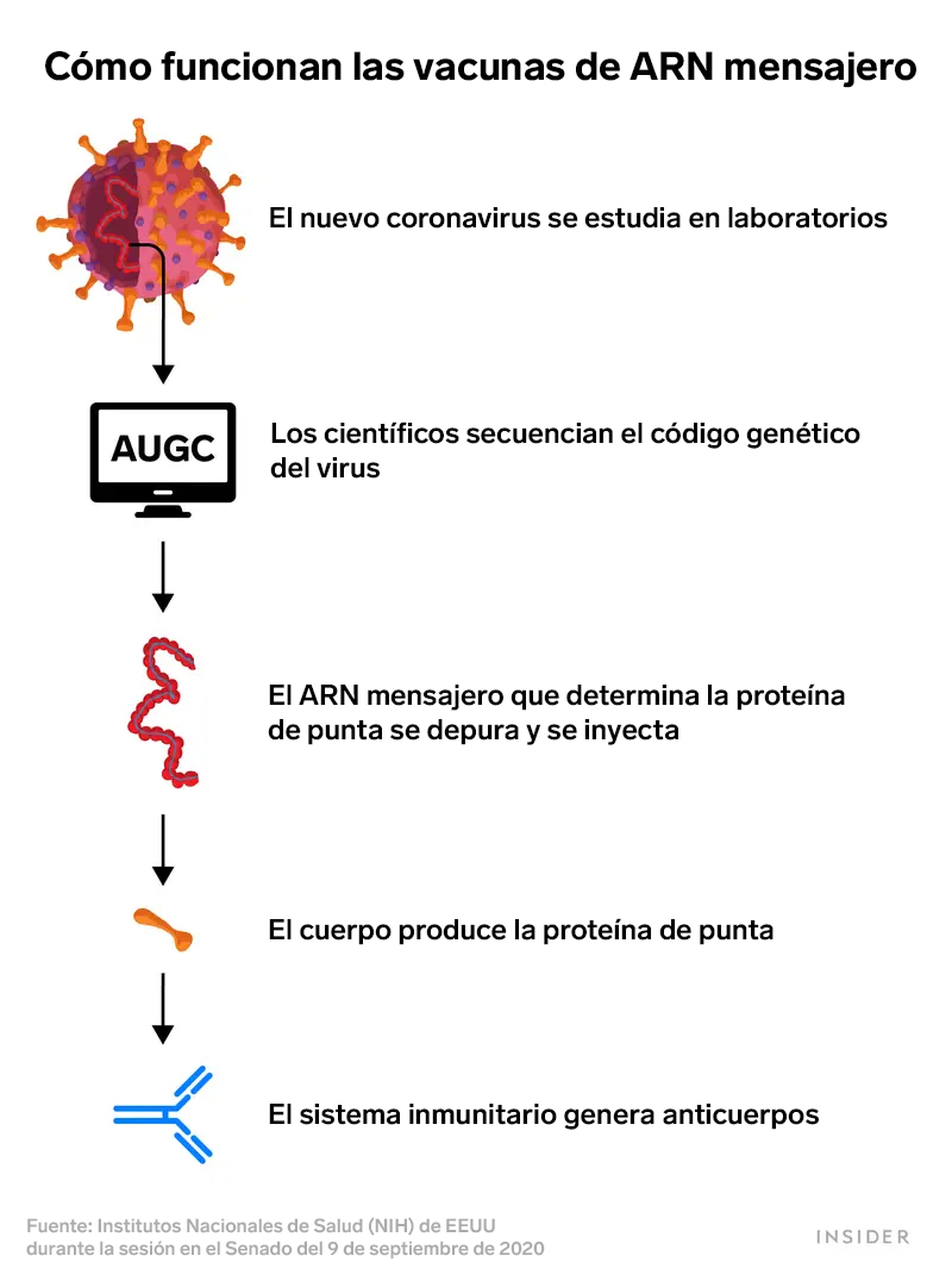
Los científicos descubrieron el ARNm por primera vez en 1961.
Aproximadamente 30 años después, investigadores de la Universidad de Wisconsin (EEUU) y la empresa biotecnológica Vical Incorporated descubrieron cómo fabricar ARNm para que instruyera a las células vivas a fabricar proteínas específicas.
En 2005, la bioquímica Katalin Karikó —ahora vicepresidenta senior de BioNTech— había descubierto cómo configurar el ARNm para que traspasar las defensas naturales del cuerpo y evitar una peligrosa respuesta inmunológica.
Ese trabajo inspiró la fundación de Moderna, que se centra únicamente en las terapias de ARNm.
Antes de la pandemia, Moderna había introducido 8 vacunas de ARNm en ensayos clínicos, incluyendo una vacuna contra la gripe.
En 2017, Karikó, junto con varios otros investigadores de BioNTech y la Universidad de Pennsylvania (EEUU), mostró que una vacuna de ARNm protegía a los ratones y monos contra el virus Zika.
Por ende, para Karikó no fue una sorpresa que 2 vacunas de ARNm fueran eficientes contra el COVID-19.
"Cuando la gente dice: "No hay ninguna vacuna de ARN mensajero que haya existido", es muy importante saber que no es porque haya fallado", destacó a Business Insider. "Simplemente no ha tenido la oportunidad de ser probada en muchas personas".
Es poco probable que se produzcan efectos secundarios a largo plazo. Son los de corto plazo los que los científicos suelen controlar y parecen ser leves y fugaces
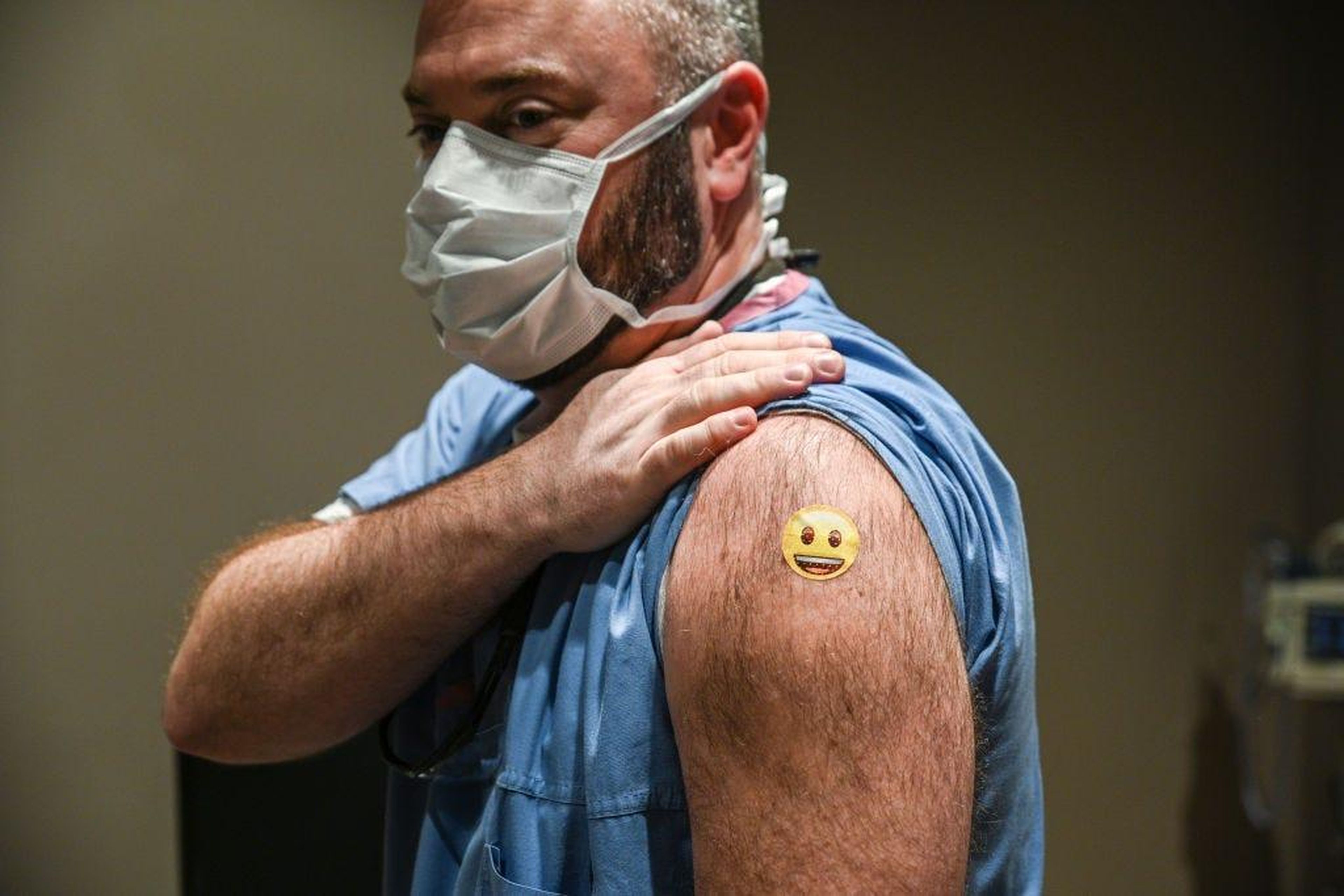
Tanto Moderna como Pfizer han hecho un seguimiento de los voluntarios de, al menos, 2 meses después de recibir su segunda inyección (ambas vacunas requieren 2 dosis).
Y, hasta el momento, no se han reportado problemas de seguridad importantes.
"Los efectos adversos documentados de las vacunas se muestran principalmente en horas, a veces en días, rara vez en semanas", escribió recientemente en Twitter Megan Ranney, directora del Centro Lifespan de Salud Digital de la Universidad de Brown (EEUU).
Con las vacunas de ARNm en particular, el cuerpo destruye la molécula con bastante rapidez, lo que significa que no se quedará en el organismo.
La mayoría de los participantes de Pfizer informaron sobre efectos secundarios temporales después de ser vacunados, como fatiga, dolores de cabeza y dolor en el lugar de la inyección.
Las personas menores de 55 años reportaron más efectos secundarios en general. Entre los voluntarios de 18 a 55 años, el 4,6% reportó fatiga severa después de recibir su segunda inyección, y el 3,2% tuvo dolores de cabeza severos.
En el ensayo de Moderna, 9 de cada 10 personas que recibieron las inyecciones registraron algunos efectos secundarios, pero en su mayoría fueron leves o moderados.
Alrededor del 17% reportó efectos secundarios más serios incluyendo dolor o hinchazón en el lugar de la inyección, fiebre, dolor de cabeza, fatiga, náuseas y vómitos. Los efectos secundarios típicamente duraban de 1 a 3 días, de acuerdo con los documentos publicados por la FDA.
Los efectos de la vacuna de Pfizer son horribles, pero merece la pena
En ambos ensayos, estos resultados fueron consistentes entre géneros, grupos de edad, grupos étnicos y raciales, y personas con problemas médicos preexistentes.
"La experiencia previa muestra que después de que una vacuna ha sido aprobada por la FDA, es raro descubrir cualquier efecto secundario serio nuevo e inesperado", explica el doctor Noam Tau, médico del Centro Médico Sheba (EEUU), en una declaración a Business Insider.
Algunas personas han sufrido reacciones alérgicas a la vacuna, pero han sido casos muy raros hasta ahora
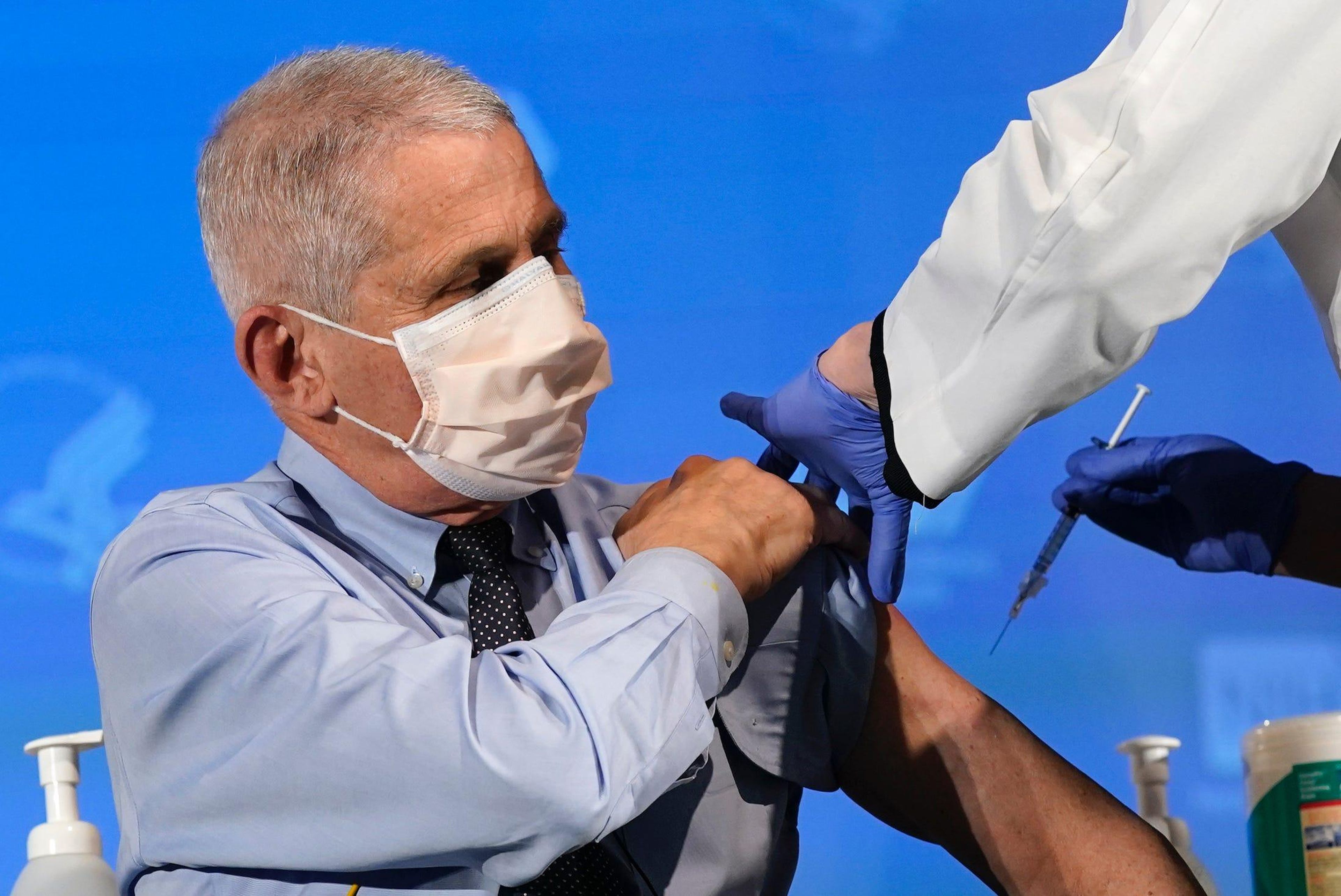
Datos recientes de los Centros para el Control y la Prevención de Enfermedades (CDC) sugieren que sólo se han registrado 29 casos de anafilaxis confirmada entre los 5 millones de estadounidenses que han recibido inyecciones de Moderna o Pfizer, por ejemplo.
La mayoría de las reacciones ocurrieron dentro de los 15 primeros minutos de la vacunación, por lo que los CDC recomiendan que los lugares de vacunación tengan epinefrina a mano.
Al menos 4 pacientes fueron hospitalizados, con problemas como sibilancias, sarpullidos y, al menos en un caso, alguna dificultad para respirar, pero todos se recuperaron.
Algunos médicos sospechan que, en casos excepcionales, las personas pueden ser alérgicas a un ingrediente llamado polietilenglicol, que se encuentra en el componente lipídico de las vacunas.
Los lípidos son sustancias grasas que ayudan al ARN a cruzar la membrana celular. Pero la mayoría de las personas ingieren este ingrediente diariamente en alimentos, cosméticos y medicamentos.
El resto de los ingredientes de la vacuna no son particularmente alergénicos: en su mayoría son sal, azúcar y algunas sustancias que ayudan a estabilizar otros ingredientes. Según Pfizer, la vacuna no contiene ningún alérgeno común como las nueces, los huevos o los metales pesados.
La FDA ha dicho que cualquier persona con alergias graves a los ingredientes de la vacuna no debe ser inmunizada.
"Las personas con alergias estacionales en general, no creo que tengan problemas con la vacuna", declaró a ABC News la doctora Erin Reigh, médica del Centro Médico Dartmouth-Hitchcock (EEUU).
Las vacunas aún no se recomiendan para ciertos grupos, como las mujeres embarazadas y los niños pequeños. Pero esto se debe a la falta de datos, no a problemas de seguridad conocidos

Pfizer ha probado su vacuna en personas de más de 12 años. Pero el tamaño de la muestra de los niños de 12 a 15 años era demasiado pequeño para sopesar los riesgos, por lo que la EMA y la FDA sólo han autorizado la vacuna en personas de 16 años en adelante.
Moderna, mientras tanto, sólo probó su vacuna en adultos de 18 años o más.
Suele ser difícil incluir a los niños en los ensayos por motivos éticos y de seguridad. Puede que los padres no se sientan cómodos inscribiendo a sus hijos en los ensayos, y los investigadores suelen preferir probar las vacunas en adolescentes antes que en niños pequeños. Pero hay pocas razones para sospechar que los niños reaccionarán mal.
"Los niños generalmente responden bien a las vacunas", cuenta a Business Insider Donna Farber, inmunóloga de la Universidad de Columbia (EEUU). "Deberían responder bien o comparablemente a un adulto joven —e incluso mejor—".
Tampoco se espera que las mujeres embarazadas respondan de manera diferente. Aunque todavía no han sido incluidas en los ensayos, la FDA dice que a las mujeres embarazadas no se les negará la vacuna contra el coronavirus si ellas y sus médicos deciden que es lo correcto.
Pfizer y Moderna tienen previsto hacer un seguimiento de las mujeres embarazadas que decidan vacunarse.
De esta manera, los expertos en salud pública han determinado finalmente que es seguro, para las mujeres embarazadas, recibir la vacuna antigripal —aunque nunca se les incluyó en los ensayos—.
Las revisiones de la FDA también han dicho que hay "datos insuficientes" para evaluar si la vacuna es segura para las personas inmunodeficientes.
A pesar de que los ensayos de etapa final incluyeron a algunas personas con problemas de salud preexistentes, la vacuna podría ser menos efectiva si el sistema inmunológico del paciente no funciona adecuadamente.
Los ensayos clínicos tienen un historial vergonzoso entre las comunidades de color, pero estos estudios se han realizado de forma segura entre un grupo diverso de voluntarios
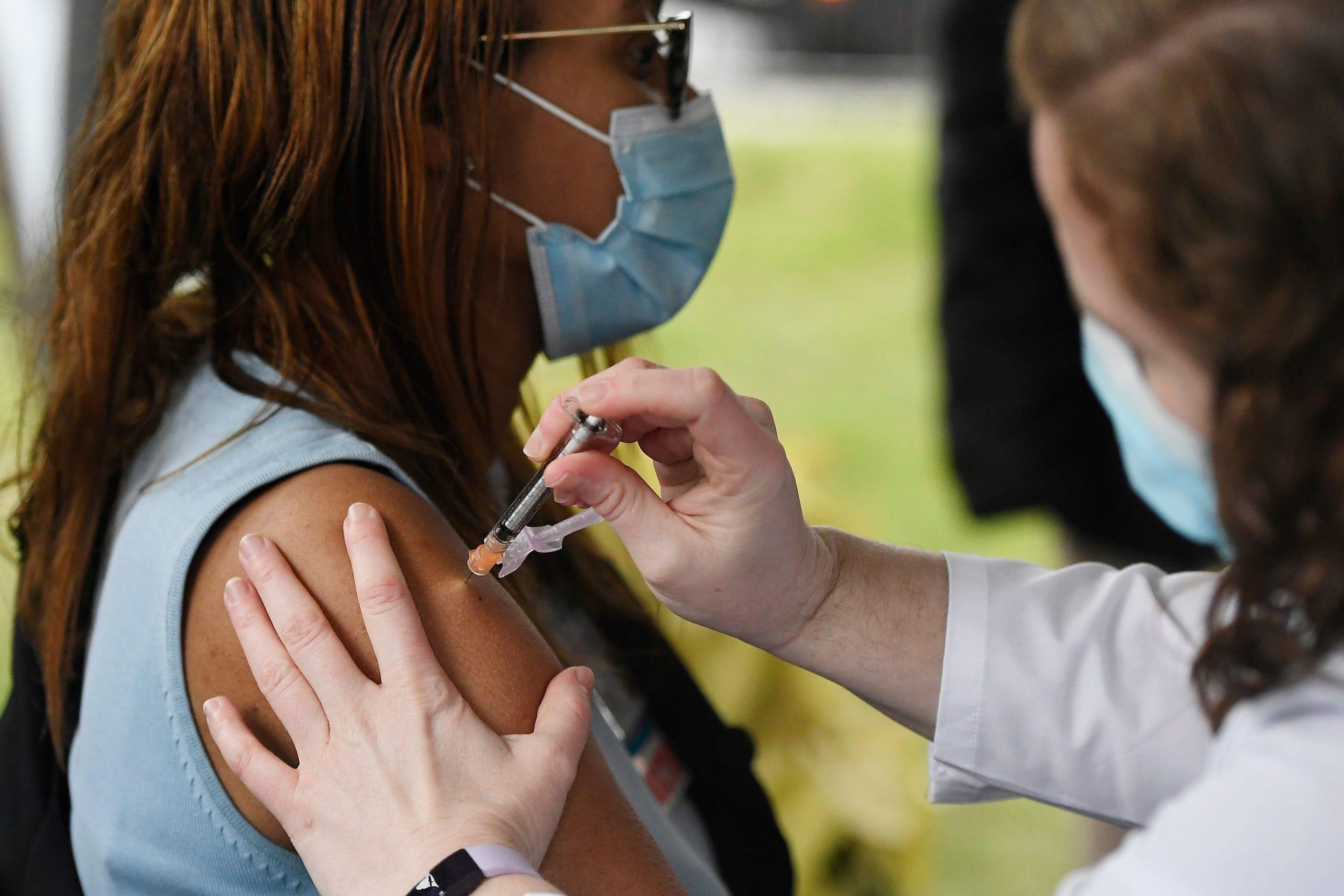
Muchas personas de raza negra siguen siendo escépticas con respecto a las vacunas, debido a una larga historia de explotación médica.
En el siglo XIX, el médico James Marion Sims realizó una serie de experimentos de salud reproductiva sin anestesia en mujeres esclavizadas. A partir de 1932, el experimento de Tuskegee, que duró 40 años, negó el tratamiento de la sífilis a los hombres negros que se habían inscrito bajo la promesa de atención médica gratuita. De 1961 a 1974, el experimento de la prisión de Holmesburg ensayó sustancias tóxicas y drogas que alteran la mente en reclusos negros de Filadelfia.
En los recientes ensayos de la vacuna contra el coronavirus se intentó incluir un grupo diverso de participantes. Moderna incluso ralentizó su ensayo en septiembre para dar más tiempo a que los voluntarios negros se unieran.
"Preferiría que tuviéramos participantes más diversos y que nos tomáramos una semana más", decía el director general de la compañía, Stéphane Bancel, a CNBC, añadiendo que la diversidad "nos importa más que la velocidad".
Por qué no estás del todo protegido del COVID-19 después de la primera dosis de la vacuna
A finales de octubre, el 37% de los participantes en el ensayo de Moderna no eran blancos. Los voluntarios hispanos/latinos constituyeron el 20% de los participantes, mientras que los voluntarios negros, el 10% y los asiático-americanos, el 4%.
Al 21 de diciembre, el 42% de los participantes en el ensayo global de Pfizer no eran blancos. Los voluntarios hispanos/latinos representaron el 26% de los participantes y los voluntarios negros el 10%. Los asiáticos eran el 5% en los ensayos, mientras que los nativos americanos representaban el 1,1%.
Los científicos están de acuerdo en que es mucho más seguro recibir una vacuna autorizada por la FDA que arriesgarse a contraer COVID-19, que tiene efectos conocidos a largo plazo
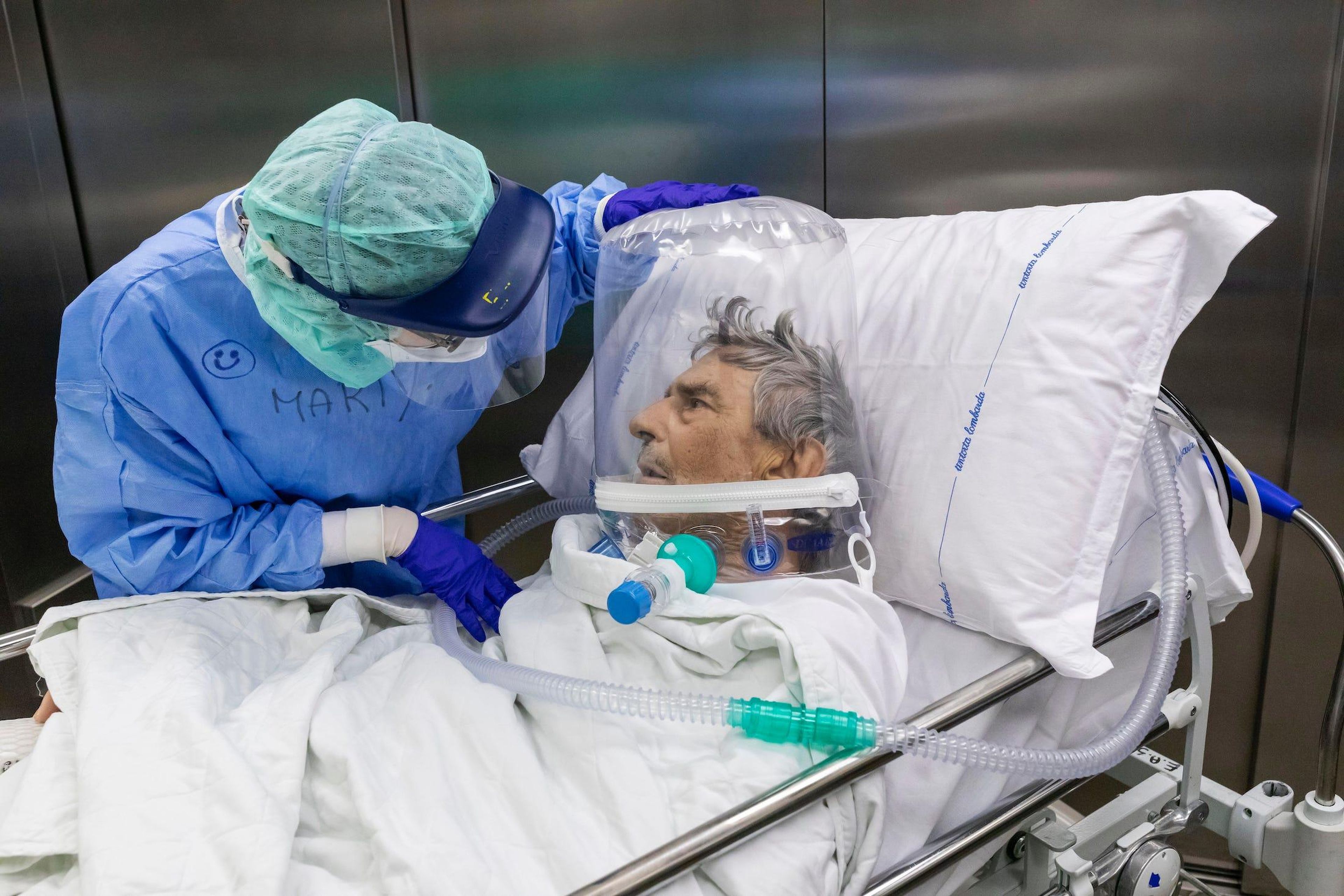
Muchos pacientes con coronavirus desarrollan secuelas a largo plazo de sus infecciones, aunque los investigadores aún no están seguros de qué parte de la población lo sufre.
Un informe de julio de los CDC encontró que cerca de un tercio de los pacientes con coronavirus encuestados no se habían recuperado después de 2 o 3 semanas. Un estudio de agosto estimó que 1 de cada 10 pacientes con coronavirus experimentaba una enfermedad prolongada.
Muchos de los afectados han luchado durante meses con fatiga, dolores musculares, problemas para respirar, palpitaciones cardíacas o dificultades para dormir. Algunos han reportado problemas neurológicos como mareos, confusión y delirio. Otros han identificado síntomas extraños como la pérdida de cabello y erupciones rojas y escamosas.
7 secuelas del COVID-19 de las que podrías no recuperarte nunca
Los pacientes de COVID-19 con síntomas de larga duración también informan sentirse débiles o con niebla después de demasiada actividad física, lo cual es una característica del síndrome de fatiga crónica, una enfermedad que puede durar varios años o más.
Un estudio de seguimiento de pacientes con SARS en Hong Kong encontró que el 27% cumplía con los criterios clínicos para el síndrome de fatiga crónica hasta 4 años después del comienzo de su enfermedad. El SARS y el nuevo coronavirus comparten alrededor del 80% de sus códigos genéticos.
8 secuelas que podrían sufrir los pacientes asintomáticos de COVID-19, según alertan los expertos
Otro estudio de 109 pacientes de SARS en Toronto, Canadá, encontró que más de la mitad no habían regresado al trabajo debido a la persistente fatiga y debilidad, un año después de haber sido dados de alta de la UCI.
"Se habla en la comunidad médica de una enfermedad similar al síndrome de fatiga crónica que podría ocurrir después de un coronavirus", explicitó a Business Insider el doctor Nate Favini, jefe médico de Forward, un consultorio de atención primaria.
"Desafortunadamente, habrá un pequeño subconjunto de personas para las que esto sea una realidad y estos síntomas realmente se transforman en algo crónico con lo que se tiene que lidiar durante años".
Conoce cómo trabajamos en BusinessInsider.
Etiquetas: EnfermedadesMedicina, Salud, Listas, Upday, Coronavirus