Los 10 tratamientos más prometedores contra el coronavirus que podrían ayudar a frenar la pandemia aunque no exista una vacuna

- Cientos de tratamientos experimentales de COVID-19 han empezado a ser probados clínicamente en los últimos meses.
- Dos de ellos, el plasma convaleciente y el remdesivir, han obtenido autorización de emergencia de la Administración de Medicamentos y Alimentos de Estados Unidos —el último, también por la Agencia Europea del Medicamento—.
- Estos son los 10 tratamientos más prometedores para la comunidad científica, incluyendo terapias de anticuerpos, plasma y medicamentos de interferón.
- Descubre más historias en Business Insider España.
El mundo sólo ha erradicado una infección en humanos: la viruela.
Así que es poco probable que el nuevo coronavirus desaparezca por completo de la población, aunque se desarrolle, apruebe y distribuya rápidamente una vacuna.
En el escenario más optimista, algunos países, como Estados Unidos y España, podrían tener lista una vacuna a finales de 2020. Pero, para entonces, se espera que las muertes lleguen hasta a duplicarse, según el modelo predictivo del Gobierno de EEUU.
Además, hasta las candidatas a vacuna más prometedoras en desarrollo enfrentan desafíos.
En septiembre, AstraZeneca detuvo su ensayo de la vacunaen fase 3, tras una reacción adversa aparente de un participante. El ensayo se ha reanudado en Reino Unido, pero sigue suspendido en Estados Unidos.
Es decir, aunque no haya retrasos ni contratiempos, la difícil tarea de producir y distribuir en masa una vacuna significa que la inmunidad de la manada está muy lejos de ser una realidad.
Eso hace que una cosa sea cierta:necesitamos tratamientos y terapias, sin importar lo que pase.
Hasta ahora, 2 de los que están en desarrollo han sido aprobados para uso de emergencia por la Administración de Drogas y Alimentos de EEUU: el plasma convaleciente y el remdesivir —también aprobado y en uso en Europa, por la Agencia Europea del Medicamento—.
Cientos más han empezado a ser probados clínicamente, desde nuevos medicamentos diseñados específicamente para combatir el virus, hasta fármacos reutilizados que inhiben una respuesta inmunológica fuera de control.
"Lo que realmente necesitamos son medicamentos que, cuando se administran a tiempo, puedan evitar que una persona sintomática requiera hospitalización o disminuyan muy dramáticamente el tiempo en que son sintomáticos", explicaba el doctor Anthony Fauci, director del Instituto Nacional de Alergia y Enfermedades Infecciosas y principal epidemiólogo al frente de la pandemia en Estados Unidos, al fundador de Facebook, Mark Zuckerberg, en julio.
Estos son los 10 tratamientos —ordenados alfabéticamente, por sus siglas en inglés— que la comunidad científica cree que son los más prometedores, hasa el momento.
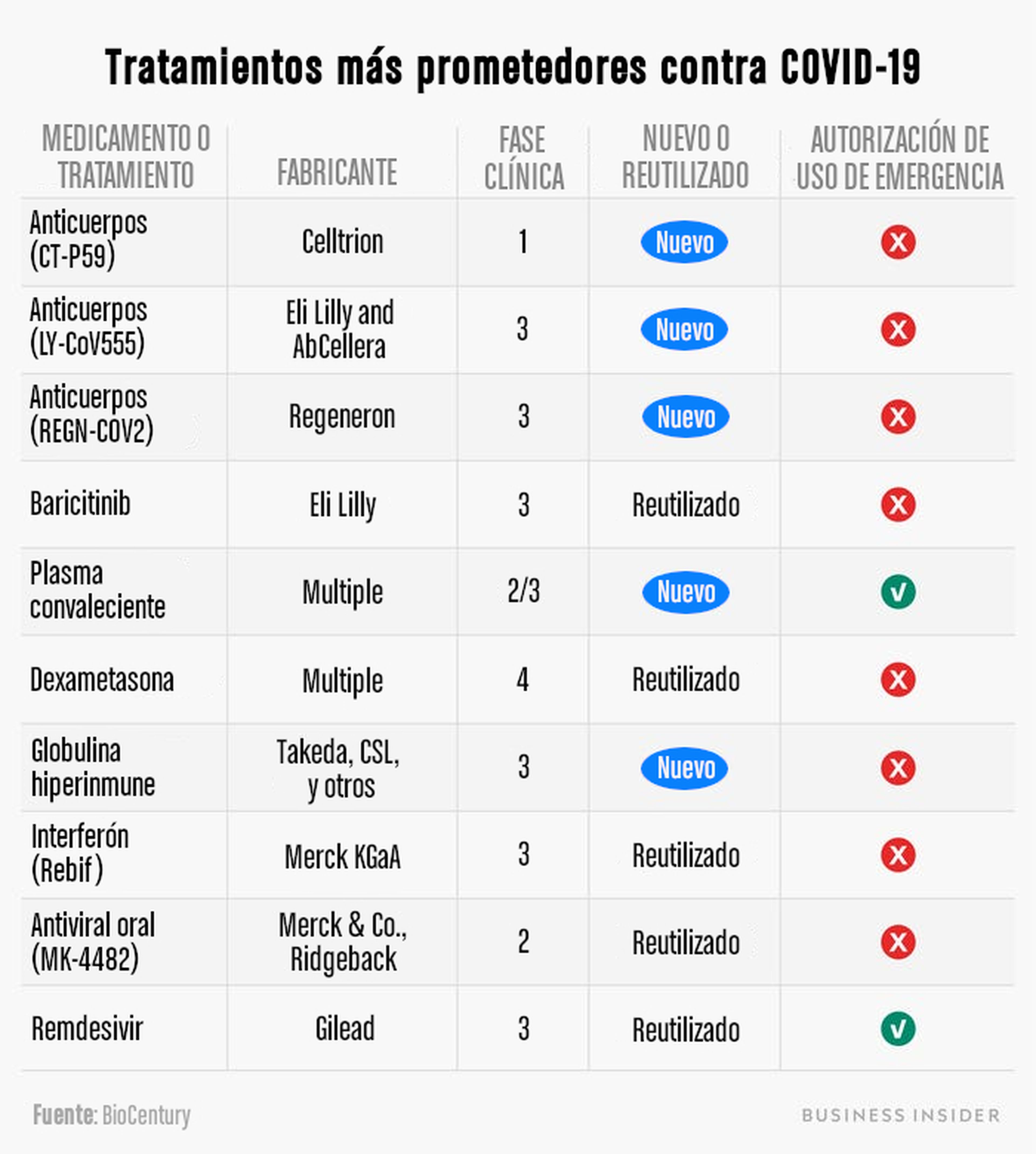
A continuación, un resumen de los principales tratamientos candidatos a combatir al nuevo coronavirus.
La terapia de anticuerpos de Celltrion usa las defensas naturales del cuerpo para combatir la infección
Muchas de las personas que contraen el nuevo coronavirus desarrollan anticuerpos neutralizantes —la respuesta natural de nuestro cuerpo a un patógeno extraño—, a los que Fauci llama "el patrón de oro de la protección contra una infección viral".
Para hacer una terapia, los científicos buscan los anticuerpos más potentes entre una gran cantidad de sangre recolectada de donaciones o de pruebas con animales. Luego clonan y producen esos anticuerpos a escala masiva.
Ahora mismo, hay cerca de 50 programas de investigación para desarrollar fármacos de anticuerpos para COVID-19.
Celltrion, una compañía biotecnológica surcoreana, ha lanzado un ensayo en humanos para su medicamento de anticuerpos, CT-P59, a mediados de julio.
El estudio es pequeño —32 voluntarios sanos— y se centrará en la seguridad del fármaco, esperando saber si es efectivo a finales de 2020.
Además, planea lanzar estudios en Europa a finales de año para ver si el medicamento puede tratar casos leves y moderados. Y otro ensayo para probarlo como herramienta preventiva podría tener resultados para el primer trimestre de 2021.
"Celltrion no debería ser nunca subestimado", escribía Ronny Gal, analista de la industria de AllianceBernstein, a los inversores en julio, añadiendo que la compañía tiene una "huella de fabricación masiva" y una capacidad demostrada para crear medicamentos anticuerpo.
Eli Lilly está probando su fármaco de anticuerpos en residencias de personas mayores en Estados Unidos
Eli Lilly, un gigante farmacéutico de 143.000 millones de dólares —más de 120.000 millones de euros—, es principalmente conocido por la venta de insulina.
Pero, ahora, la compañía tiene 2 candidatos de anticuerposcontra el coronavirus en pruebas en humanos.
El más avanzado es el LY-CoV555, desarrollado con AbCellera, una pequeña empresa biotecnológica canadiense.
En agosto, Eli Lilly inició un ensayo clínico de última etapapara probar el medicamento en residentes y miembros del personal de residencias de personas mayores en EEUU. Y sostiene que el ensayo incluirá hasta 2.400 personas para ver si el medicamento puede prevenir infecciones en lugares donde se han confirmado casos recientemente.

Los datos de si el fármaco funciona, o no, se esperan para el cuarto trimestre de 2020, según Eli Lilly, que espera tener varios cientos de miles de dosis del tratamiento disponibles para finales de este año.
En una entrevista con Insider, Bill Gates dijo que los medicamentos de anticuerpos podrían "reducir la tasa de mortalidad de forma bastante drástica" entre los pacientes de coronavirus.
Regeneron es líder en la creación de terapias de anticuerpos
La biotecnológica Regeneron ha diseñado ratones para producir anticuerpos que imitan el sistema inmunológico humano a través de una plataforma tecnológica llamada VelocImmune.
Dicha tecnología ha conseguido varios fármacos aprobados, incluyendo uno de anticuerpos contra el Ébola que ayuda a reducir el riesgo de muerte de los pacientes.
En junio, Regeneron empezó las pruebas clínicas para el REGN-COV2, su cóctel de 2 anticuerpos.
Estos ensayos iniciales se centran en pacientes que ya tienen el coronavirus —mientras, uno se administra a pacientes hospitalizados y otro para casos menos graves, no hospitalizados—. Según la compañía, en julio, los datos de los primeros 30 pacientes sugirieron que el medicamento podría ser seguro para los humanos.
Leer más: Las vitaminas que pueden ayudar a reforzar tu sistema inmunológico
Este 29 de septiembre, Regeneron publicó una descripción de los resultados de los primeros 275 voluntarios del estudio de pacientes no hospitalizados. Con estos, el director científico George Yancopoulos afirmó que aseguraban la creencia de la bioteconológica de que el fármaco tiene más probabilidades de beneficiar a las personas que no presentan una respuesta inmunológica antes de tomarlo.
Asimismo, otros estudios se centran en evaluar la capacidad preventiva del REGN-COV2; con un ensayo que arrancó en julio de este mismo año. El estudio está diseñado para probar en personas que tienen una exposición cercana al virus, como alguien que vive con un infectado. Los investigadores esperan inscribir a unos 2.000 participantes en 100 lugares diferentes.
Eli Lilly también está probando una sustancia para la artritis reumatoide
La comunidad científica ha desarrollado varias teorías acerca de por qué los casos de coronavirus pueden convertirse rápidamente en graves.
Una es que un exceso de señales químicas puede instruir al cuerpo para atacar a sus propias células —lo que se conoce como "tormenta de citoquinas"—.
Un tipo de medicinas antiinflamatorias llamadas inhibidores de la quinasa Janus (JAK) ayudan a calmar esta tormenta bloqueando la producción de citoquinas. Y ya se usan para tratar la artritis reumatoide, una de las enfermedades con las que tu cuerpo se ataca a sí mismo.
Uno de estos medicamentos para la artritis, el baricitinib de Eli Lilly, está aprobado para tratar adultos con artritis reumatoide moderada a severa en más de 70 países.
Actualmente, este se muestra también prometedor como un tratamiento para COVID-19 cuando se combina con otro de los ya aprobados: el remdesivir de Gilead Sciences.
La combinación de ambos entró en la fase 3 de un ensayo clínico en mayo que involucra a más de 1.000 pacientes hospitalizados con COVID-19.
En septiembre, Eli Lilly ya anunció que juntos, el baricitinib y el remdesivir redujeron el tiempo promedio de recuperación de los pacientes en un día en comparación con los pacientes que sólo recibieron el remdesivir. Los resultados pusieron a la compañía un paso más cerca de buscar una autorización de emergencia de la FDA de EEUU.
El plasma convaleciente podría evitar que los casos leves se vuelvan severos
La FDA en EEUU emitió una autorización de emergencia para este tratamiento el pasado 23 de agosto.
La terapia de plasma convaleciente se remonta a la pandemia de gripe de 1918, cuando ayudó a reducir la mortalidad entre las personas con infecciones agudas.
Dado que los anticuerpos se desarrollan en el plasma, la porción líquida de la sangre, los médicos pueden transferir este plasma por vía intravenosa a un paciente con coronavirus. Esto debería incitar al nuevo paciente a desarrollar una respuesta de anticuerpos, lo que podría evitar que un caso leve se volviera más grave.
Hasta ahora, un estudio de la Clínica Mayo que aún está pendiente de revisión por pares, encontró que la terapia de plasma podría reducir la mortalidad entre los pacientes hospitalizados en un 57%.
Y en una investigación que involucró a 5.000 adultos con casos severos o que amenazaban su vida, los investigadores de la Clínica Mayo determinaron que el tratamiento era relativamente seguro.

La autorización de emergencia en EEUU permite a los médicos administrar el tratamiento en una etapa temprana del curso de una infección, cuando se cree que es más eficaz.
Pero el doctor Thomas File, presidente de la Sociedad de Enfermedades Infecciosas de América, sostiene que los datos disponibles sobre el tratamiento son todavía insuficientes.
"Si bien los datos hasta la fecha muestran algunas señales positivas de que el plasma convaleciente puede ser útil para tratar a los individuos con COVID-19, especialmente si se administra al principio de la trayectoria de la enfermedad, carecemos de los datos de los ensayos necesarios, controlados aleatoriamente, para comprender mejor su utilidad en el tratamiento de COVID-19", argumentaba File en una declaración el 23 de agosto.
Más de 2.700 hospitales estadounidenses ya han administrado la terapia de plasma a través de un programa de acceso expandido dirigido por la Clínica Mayo.
Asimismo, según su web, el programa ha administrado plasma a más de 105.000 pacientes, pero suspendió el registro una vez se anunció la autorización de la FDA.
La dexametasona es una opción barata para los pacientes con casos agudos
Una de las mayores sorpresas en la investigación de COVID-19 hasta ahora, ha sido la dexametasona.
Los responsables de un importante ensayo clínico en el Reino Unido descubrieron que el esteroide genérico y barato, reducía significativamente la posibilidad de que un paciente gravemente enfermo muriera.
Los autores del estudio dijeron que la dexametasona redujo el número de muertes en un tercio para las personas en respiradores, y en un 20% entre los pacientes con COVID-19 que recibían oxígeno extra.
"Cuando se tiene una enfermedad avanzada, es menos el virus el que hace daño que la respuesta inflamatoria anormal, que es la razón por la que la dexametasona funciona", decía Fauci en julio.
El Gobierno de Reino Unido ha autorizado el uso de dexametasona como tratamiento estándar para los pacientes gravemente enfermos de COVID-19.
Las directrices de tratamiento de los Estados Unidos también recomiendan el uso del esteroide en pacientes que están en respiradores o necesitan apoyo de oxígeno, aunque la FDA no ha emitido una autorización de uso de emergencia.
La globulina hiperinmune podría hacer ganar tiempo hasta que una vacuna llegue al mercado
En mayo, una coalición de instituciones médicas, compañías farmacéuticas, organizaciones sin ánimo de lucro y supervivientes de COVID-19 lanzaron "The Fight Is In Us" ("La lucha está en nosotros", en su traducción al castellano), una campaña para conseguir que más pacientes con coronavirus recuperados donaran sangre.
Parte de esa sangre se destinará a transfusiones directas. El resto, a la fabricación de globulina hiperinmune, un fármaco hecho a partir de plasma de convalecientes, explica el grupo.
La creación de la globulina hiperinmune implica reunir el plasma de los pacientes recuperados y tratarlo con calor para destruir los patógenos restantes.
Leer más: Todo lo que se sabe sobre la posibilidad de ser inmune al COVID-19 sin haber pasado la enfermedad
El resultado es un frasco de medicamento con niveles de anticuerpos consistentes que puede ser fácilmente administrado a los pacientes. El fármaco se centra en el anticuerpo más común que se encuentra en la sangre: la inmunoglobulina G o IgG, que suele conferir inmunidad a largo plazo.
La compañía farmacéutica más grande de Japón, Takeda, y una biotecnológica de Pensilvania llamada CSL Behring lideran una coalición de 10 compañías farmacéuticas involucradas en la campaña. Esperan determinar si la globulina hiperinmune mejora los resultados de los pacientes con casos graves de coronavirus.
"Nuestra meta aquí no es continuar produciendo globulina hiperinmune ad infinitum", ha contado ya con anterioridad a Business Insider Christopher Morabito, jefe de investigación y desarrollo de terapias basadas en plasma en Takeda.
"Nuestro objetivo aquí es tener una terapia efectiva para tender un puente hasta un punto en el que la pandemia termine porque se extinga, porque haya una vacuna disponible, o hasta que haya muchos tratamientos más efectivos para los pacientes con esta enfermedad".
La coalición espera asegurar la aprobación de la FDA a finales de 2020.
El fármaco interferón de Merck KGaA se está combinando con otras terapias prometedoras
Los interferones son la primera línea de defensa de nuestros cuerpos contra el coronavirus. Pero las primeras investigaciones han sugerido que el virus podría desactivar estas proteínas, lo que llevaría a una respuesta inmunológica aún más agresiva.
Los fabricantes de medicamentos están probando si un aumento de interferones podría ayudar a evitar una infección grave.
Los médicos ya usan Rebif, una inyección de interferón de la compañía biofarmacéutica alemana Merck KGaA, para tratar a los pacientes que recaen en la esclerosis múltiple.
Leer más: Por qué puedes ser inmune al coronavirus aunque los anticuerpos desaparezcan
Ahora, la compañía espera que el fármaco también impida que el coronavirus se replique en los humanos y reduzca la inflamación.
Está siendo probado en conjunto con otras terapias como el lopinavir (un antiviral contra el VIH) y el remdesivir, que fue desarrollado como un tratamiento para el Ébola.
Este agosto, el Instituto Nacional de Alergia y Enfermedades Infecciosas de EEUU lanzó un ensayo de fase 3 para ver si el Rebif y el remdesivir podrían acortar los tiempos de recuperación de los pacientes con coronavirus. Este, que espera inscribir a 1.000 pacientes, podría dar resultados preliminares este otoño.
La pastilla antiviral de Merck podría ser administrada justo después de que alguien dé positivo
Los antivirales funcionan apuntando a un virus para evitar que se replique dentro del cuerpo. Algunos investigadores piensan que como estos medicamentos ya se utilizan para tratar la gripe y el VIH, podrían representar el futuro del tratamiento contra el coronavirus.
"Tan pronto como alguien llega con una prueba positiva, bingo, le das un antiviral y listo. Eso es lo que veo para el futuro", sostuvo Fauci en agosto.
"Sinceramente, no hay ninguna razón por la que no podamos hacer eso. No hay razón para que eso no sea posible. Diablo, si lo hicimos para el VIH, podemos hacerlo para el coronavirus".
Leer más: Cómo tratar el norovirus y cuánto tiempo debería durar la enfermedad
La compañía farmacéutica Merck & Co. está trabajando con una compañía biotecnológica llamada Ridgeback Biotherapeutics para desarrollar MK-4482, un antiviral administrado en forma de píldora. Se ha descubierto que la pastilla, originalmente diseñada como tratamiento para la gripe, evita que múltiples coronavirus se repliquen en ratones.
Otras investigaciones han encontrado que podría prevenirque el nuevo coronavirus se replique en células humanas dentro de un laboratorio —pero eso no significa necesariamente que funcione en pacientes—.
El ensayo de la segunda fase del fármaco está previsto que termine ahora, y Merck planea lanzar 2 ensayos de fase 3 para estudiar los efectos del medicamento tanto en pacientes hospitalizados con coronavirus como en pacientes ambulatorios con coronavirus. El objetivo es ver si el tratamiento acorta los síntomas o evita que los casos empeoren.
En una llamada realizada en julio a los inversores, el jefe de investigación de Merck, Roger Perlmutter, dijo que la compañía podría estar lista para entregar "millones de dosis" antes del próximo año.
Remdesivir fue el primer tratamiento aprobado para uso de emergencia, en norteamércia y Europa
El medicamento recibió autorización de emergencia para tratar el COVID-19 el 1 de mayo, en Estados Unidos, y a finales de junio en Europa.
El Remdesivir ya había sido probado en pacientes con Ébola y se constató que era seguro para los humanos. Los estudios han encontrado que el medicamento, en el que la compañía ha estado trabajando desde 2009, podría ayudar a los pacientes hospitalizados de COVID-19 a recuperarse más rápido.

Pero una investigación publicada en Journal of the American Medical Association encontró que a los pacientes que tomaron un tratamiento de 10 días de remdesivir no les fue mucho mejor que a los pacientes que no recibieron el medicamento en absoluto.
Ambos grupos de pacientes murieron al mismo ritmo, y los afectados que tomaron remdesivir experimentaron síntomas y efectos secundarios más leves o moderados (aunque informaron de menos síntomas graves en general).
En base a estos hallazgos, algunos expertos médicos sugirieron que el uso generalizado de remdesivir podría no compensar el coste.
Por su parte, Gilead, después de donar su suministro de medicamentos durante 2 meses, anunció en junio que cobraría a los Gobiernos de los países desarrollados 2.340 dólares (unos 2.090 euros) por un ciclo de 5 días de remdesivir.
En agosto, presentó el remdesivir para la aprobación oficial de la FDA para el tratamiento de COVID-19. Mientras, prueba una versión inhalada del medicamento con la esperanza de ponerlo a disposición de los pacientes no hospitalizados.
Aunque el remdesivir y la dexametasona se consideran los 2 mayores avances en los tratamientos del coronavirus hasta ahora, el panorama de los medicamentos cambia constantemente.
De hecho, la publicación de la industria BioCentury ofrece una lista completa de las terapias que se están desarrollando para COVID-19. Es posible que otros medicamentos de esa lista puedan adelantarse en los próximos meses.
Conoce cómo trabajamos en BusinessInsider.
Etiquetas: EnfermedadesMedicina, Salud, Ciencia, Coronavirus